Última actualización: 20 de julio de 2021
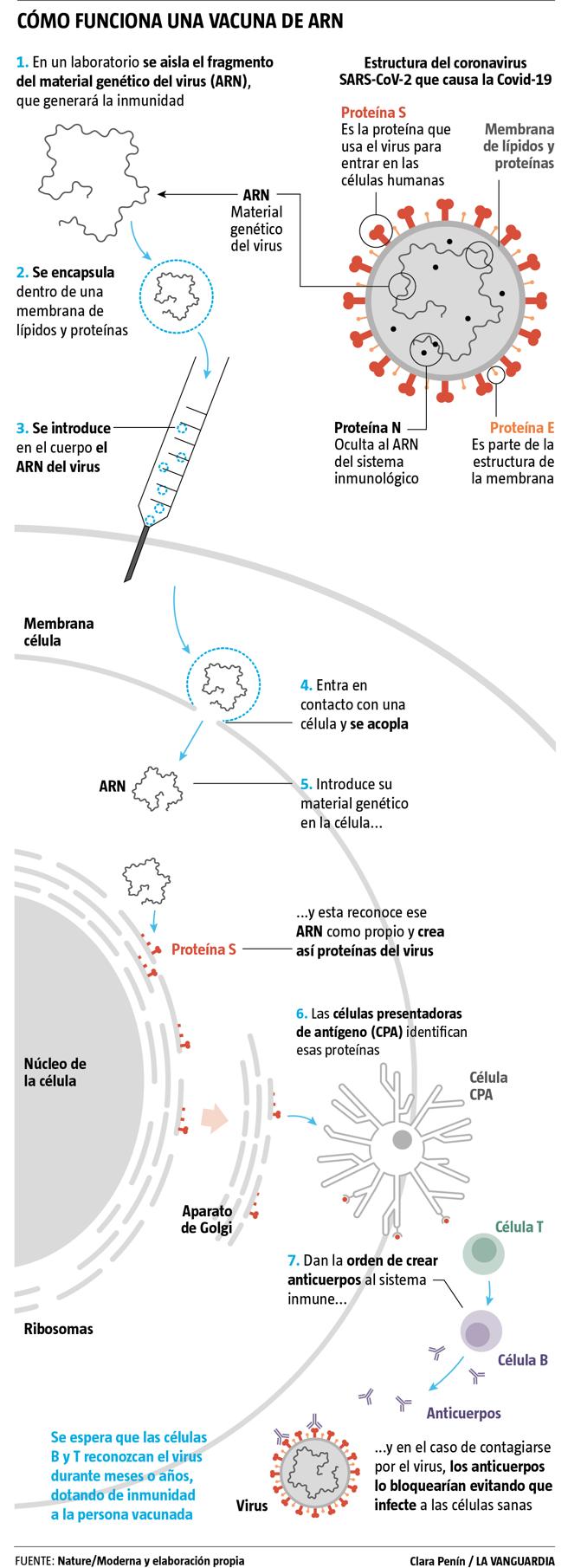
Desde el inicio de la pandemia se trató de desarrollar una vacuna contra el reloj para hacer frente al SARS-CoV-2. En concreto, se han estado elaborando vacunas de ADN/ARN, vectores virales, unidades muertas o atenuadas del virus, o vacunas de proteínas. En la siguiente infografía puedes ver las claves de cada uno de estos tipos de vacunas. Más adelante se detallan aspectos más técnicos sobre el funcionamiento de las vacunas aprobadas y candidatas.
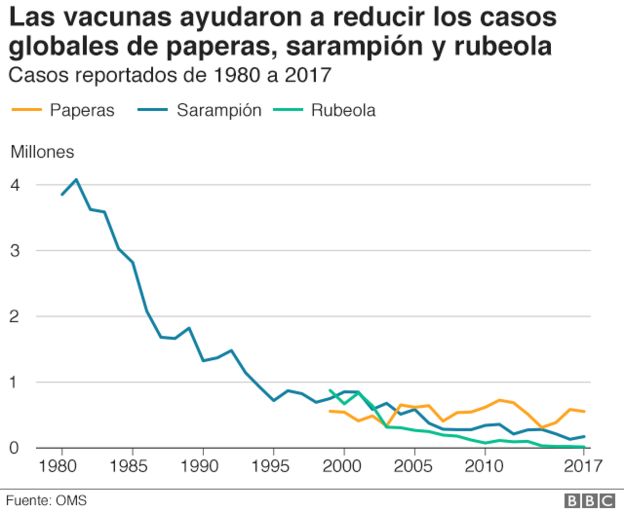
Pese a que hoy en nuestros días hay un importante movimiento antivacunas, hay evidencia científica de que han contribuido a disminuir y en algunos casos casi erradicar enfermedades que en el pasado causaban estragos entre la población mundial. El último ejemplo fue en agosto de este mismo año, cuando la OMS declaró el continente africano libre de poleomelitis (ver noticia).
Una de las fotos más icónicas a nivel mundial que ilustra la efectividad de las vacunas es la que puedes ver a continuación, tomada en Leicester en 1901 por el doctor Allan Warner. Dos chicos, uno de ellos vacunado contra la viruela, y el otro que no había sido vacunado y había desarrollado la enfermedad.
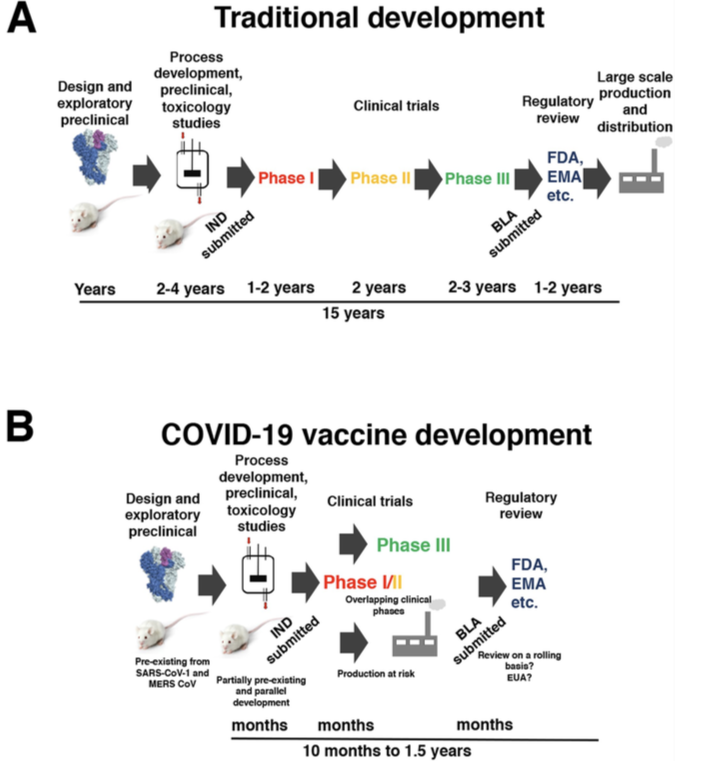
Para que haya una vacuna efectiva, tras su desarrollo, estas tienen que pasar un periodo de pruebas, ser aprobadas y homologadas. En concreto, deben de someterse a varias fases, incluyendo una fase inicial de pruebas in vitro y en animales (fase preclínica), otra de pruebas en pequeños grupos de menos de 100 personas sanas para confirmar que es segura y efectiva y comprobar posibles efectos secundarios y cuál es la dosis recomendable (fase 1), una tercera fase en la que participan más personas (fase 2), y una cuarta con miles de personas en la que se comprueba la efectividad y seguridad (fase 3). En agosto, Rusia y China habían aprobado vacunas sin superar la fase 3 de ensayos, lo que para muchos expertos suponía entonces un riesgo de seguridad para la población, y podría aumentar el descrédito hacia las vacunas si surgieran problemas. Cuando se lanza y empieza a vacunar a la población general, entra en fase 4 (farmacovigilancia).
Tras la aprobación y autorizaciones pertinentes, habría que fabricar vacunas a gran escala, puesto que habrá una gran demanda mundial. Esto abre incógnitas sobre la posibilidad de acceso a las mismas en el corto plazo, así como el precio que pudieran alcanzar. Además, la vacuna debería poder ser efectiva contra todas las variantes del virus que pudiera haber; en este sentido, las numerosas mutaciones del virus no parecían ser lo suficientemente significativas, lo cual sugería que con gran probabilidad, una única vacuna debería ser eficaz contra todas las cepas circulantes del virus (ver estudio).
En condiciones normales, una vacuna puede tardar hasta diez o quince años en desarrollarse, incluyendo varios años de pruebas. Sin embargo, en el caso de la COVID, las primeras empezaron a administrarse tras su aprobación en menos de un año. En este gráfico comparativo publicado en Nature puedes ver el enorme lapso de tiempo que llevó conseguir determinadas vacunas: más de un siglo para la fiebre tifoidea, casi un siglo para la meningitis, más de cuarenta años para el ébola... Otras se consiguieron en menos años, pero ninguna de forma tan rápida como esta.
Sin embargo, con este virus se produjo una carrera mundial con muchos candidatos, con prisas para obtener vacunas, reduciendo los plazos incluso de los ensayos clínicos, e incluso en algunos casos saltándose la fase 3 de pruebas, lo cual fue bastante criticado entre la comunidad científica. En un artículo publicado en The Lancet (ver articulo), científicos instaron a todos los reguladores a ceñirse a las recomendaciones establecidas por la OMS, de forma que no debería aprobarse ninguna vacuna con una eficacia inferior al 30%, siendo recomendable al menos un 50% de efectividad. A final de 2020 se consiguieron las primeras vacunas, desarrolladas en un tiempo récord, pero evidentemente, sin saber su eficacia real a largo plazo.
Se pusieron en marcha cientos de proyectos, algunos ya aprobados y otros en desarrollo en distintas fases. Los países con más proyectos son Estados Unidos y China (Cansino & Instituto de Biotecnologías de Pekín, Sinopharm & Institoto de Productos Bioloógicos de Wuhan/Pekín, Instituto de Biología Médica), aunque también hay proyectos avanzados en Reino Unido, Rusia, Alemania, Corea del Sur, India, Canadá o Japón. También hay varios proyectos españoles. (ver noticia)
Desde el verano de 2020, la carrera por la vacuna se aceleró, sucediéndose multitud de noticias, como las siguientes:
- El 14 de julio de 2020, la compañía farmacéutica Moderna anunció que, tras probar por primera vez su vacuna en desarrollo en humanos, todos ellos generaron anticuerpos, lo cual no significaba necesariamente que sea efectiva, pero sí que suponía un hito importante. Además, los efectos secundarios no fueron lo suficientemente dañinos como para imposibilitar más estudios (ver noticia). Esto supuso que las acciones de la compañía se dispararan un 14% en bolsa (ver noticia)
- Del mismo modo, el 15 de julio de 2020, se anunción que la vacuna desarrollada por la Universidad de Oxford y AstreZeneca estaba dando resultados positivos, de forma que conseguiría que produjera los anticuerpos y células T deseadas, a falta de nuevas pruebas. Análogamente, la compañía AstreZeneca se disparó en bolsa con esa noticia (ver artículo)
- El 20 de julio de 2020, Pfizer y CanSino también informaban de importantes progresos en sus respectivas vacunas (ver artículo).
- El 24 de julio Sinopharm anuncia que su vacuna estaba en fase 3 y podría estar lista a finales de año (ver noticia)
- El 25 de julio, Rusia anunciaba que su vacuna podría estar lista para ser usada en agosto (ver noticia), y días más tarde se anunciaba que en octubre se suministraría gratuitamente a su población (ver noticia)
- El 30 de julio se sabía que la vacuna desarrollada por Johnson & Johnson proporcionaba una respuesta robusta al generar anticuerpos neutralizantes (ver noticia)
- El 4 de agosto se informa de resultados positivos de la vacuna de Novavax (ver noticia)
- El 15 de agosto Rusia informa de que se ha producido el primer lote de su vacuna Sputnik V (ver noticia), e India informa de que está probando tres posibles vacunas (ver noticia)
- El 17 de agosto se conoce que la farmacéutica china CanSino registra la patente de su vacuna (ver noticia)
- El 18 de agosto Sinopharm anuncia que su vacuna estará lista en diciembre (ver noticia)
- El 25 de agosto se informó de que España comprará 30 millones (con opción a otros 10 millones más) de dosis de la vacuna de Oxford-AstraZeneca (ver noticia), a través de la Unión Europea.
- El 26 de agosto se informa de que la vacuna de Pfizer y BioNtech podría estar lista en octubre (ver noticia)
- El 29 de agosto se conoce que China aprueba el uso de una de sus vacunas en desarrollo, sin pasar por la fase 3 (ver noticia)
- El 5 de septiembre, The Lancet publicó que los resultados de la vacuna rusa Sputnik V son alentadores, generando anticuerpos y sin efectos adversos graves, pero que los datos conocidos aún son limitados (ver artículo)
- También el 8 de septiembre se supo que en China cientos de miles de personas habrían sido vacunadas con dos tipos de vacunas experimentales, sin haberse dado ni un caso de infección (ver artículo)
- El 9 de noviembre la farmacéutica Pfizer anunció que su vacuna podía tener una efectividad del 90% (ver noticia). Esta noticia fue acogida con gran expectación y alegría en todo el mundo, provocando subidas masivas en la bolsa y un optimismo desbordado, quizás desmedido, pues siempre hay que ser cauto.
- El 9 de noviembre también se supo que en Brasil se suspendían los ensayos de la vacuna china Sinovac al haberse producido a finales de octubre un efecto adverso grave (ver noticia).
- El 11 de noviembre Rusia anunció que su vacuna Sputnik V, fue eficaz en el 92% de los casos (ver noticia).
- El 18 de noviembre Pfizer elevaba al 95% la efectividad de su vacuna, tras haber 170 casos de la enfermedad en su ensayo de más de 43.000 voluntarios. De ellos, 162 se observaron en el grupo de control (placebo) y 8 en el grupo de vacuna. Diez personas desarrollaron covid-19 grave, una de las cuales recibió la vacuna. (ver noticia)
- El 27 de noviembre, AstraZeneca subía la efectividad de su vacuna del 70% al 90%, despertando recelo estos datos porque no habían participado mayores de 55 años (ver noticia).
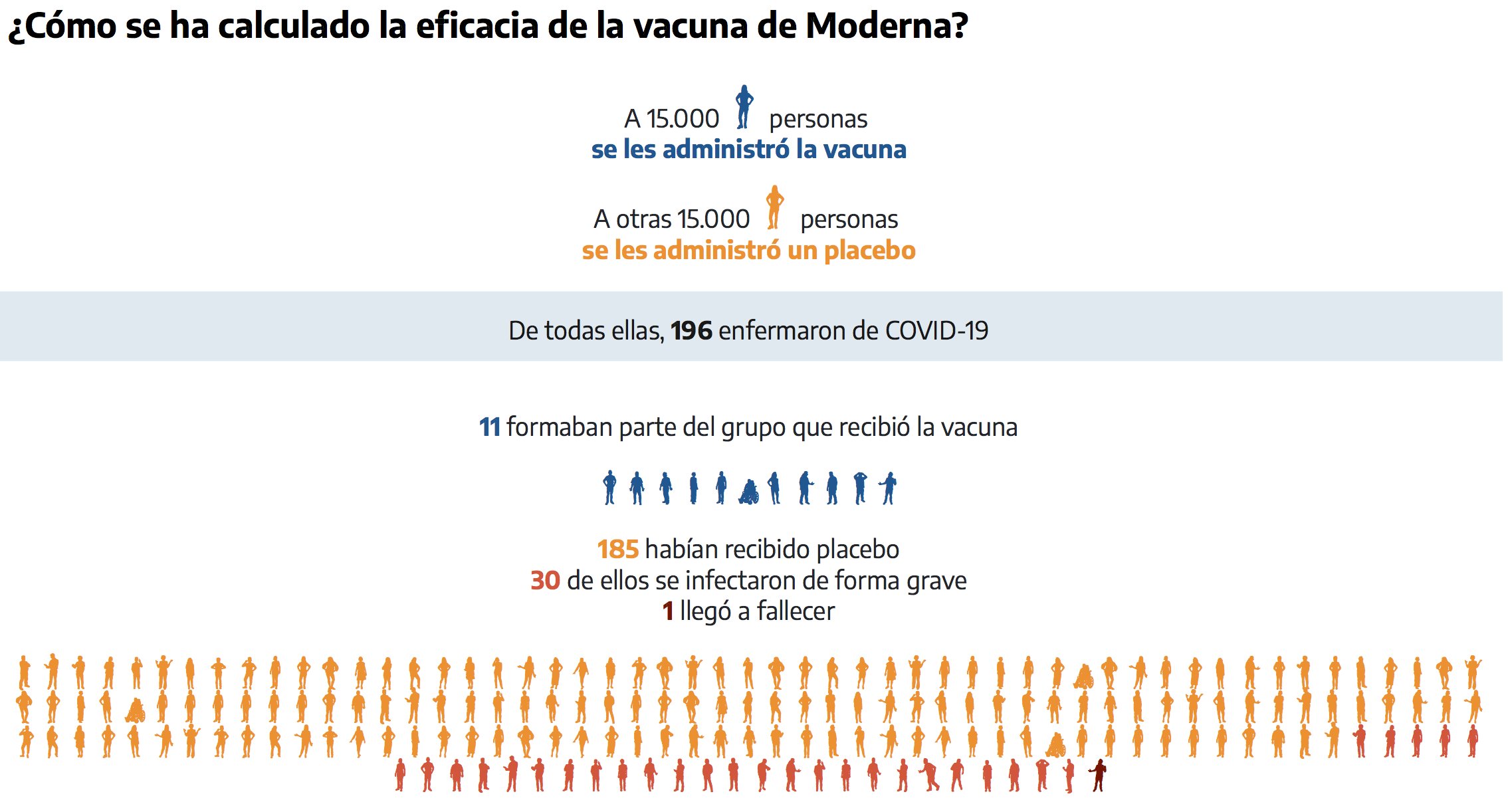
- El 30 de noviembre Moderna anunciaba que nadie de las 30.000 personas que recibió la vacuna había desarrollado COVID-19 severo, y que solo 11 de ellos se habían infectado y desarrollado síntomas, frente a 185 del grupo de control (que recibieron el placebo), lo que supone una eficacia del 94,1% (ver noticia). Ese mismo día informó de que iba a solicitar formalmente ante la FDA (Agencia del Medicamento de EEUU) la autorización de uso de emergencia, y una autorización de comercialización condicional con la Agencia Europea de Medicamentos (EMA).
Fuente: Eldiario.es
- El 1 de diciembre se conoció que la Unión Europea esperaba aprobar las vacunas de Pfizer y moderna el 29 de diciembre y el 12 de enero (ver noticia)
- El 2 de diciembre Reino Unido aprobaba la vacuna de Pfizer y BioNtech, y esperaba comenzar la vacunación antes de final de año (ver noticia)
- El 7 de diciembre la OMS se posiciona en contra de una vacunación obligatoria de la población (ver noticia)
- El 8 de diciembre comenzó la vacunación de la población en el Reino Unido (ver noticia)
- El 9 de diciembre el Reino Unido recomendaba no vacunarse a personas con alergias severas, tras las primeras reacciones producidas (ver noticia). Por tanto, la vacuna no estaría indicada para estas personas alérgicas, así como tampoco para embarazadas y menores de 16 años.
- El 11 de diciembre la compañía australiana CSL anunció la suspensión de las pruebas de su vacuna candidata tras la detección de varios participantes que en fase 1 dieron falsos positivos en las pruebas para detectar el VIH debido a los anticuerpos generados por la vacuna (ver noticia).
- El 18 de diciembre, la FDA de Estados Unidos autorizó la vacuna de Moderna, también basada en ARN mensajero (ver noticia), de la que se publicó un estudio que aseguraba que era eficaz en adultos mayores (ver estudio), pues los eventos adversos asociados con la vacuna fueron principalmente leves o moderados, y la dosis suministrada indujo la producción de anticuerpos neutralizantes. Ese mismo día, se anunciaba el comienzo de la vacunación en España para el 27 de diciembre (ver noticia).
- El 26 de diciembre llegan las primeras vacunas a España
- El 27 de diciembre se producen las primeras vacunaciones en España (ver noticia)
- El 30 de diciembre se produce la aprobación de la vacuna de Oxford-AstraZeneca en el Reino Unido (ver noticia)
- El 28 de enero de 2021 Novavax anuncia una eficacia de casi el 90% en su vacuna, reducida al 83% en el caso de la variante británica B.1.1.7, y entre el 50-60% para la emergente variante sudafricana (ver noticia).
- El 29 de enero se supo que la vacuna monodosis de Janssen (Johnson & Johnson), ofrecía una protección sólida, pero generaba preocupación porque decaía con las variantes emergentes, ya que su eficacia se redujo del 72% en los Estados Unidos a solo el 57% en Sudáfrica (ver noticia).
- El 2 de febrero, se informaba de que la vacuna Sputnik V rusa mostraba una eficacia del 91'6% en base a datos de casi 20.000 voluntarios que recibieron la primera y segunda dosis o un placebo. El ensayo incluyó a 2.144 mayores de 60 años y la eficacia fue del 91'8% en este grupo, siendo bien tolerada y mostrando síntomas gripales y reacción local inflamatoria como síntomas comunes (ver noticia).
- El 8 de febrero se anunciaba que la vacuna monodosis de CanSino (China) tenía una eficacia del 65,7% (ver noticia).
- El 26 de febrero de 2021, la FDA estadounidense afirmaba que los viales congelados de la vacuna de Pfizer se podía transportar y almacenar a temperaturas de congelación convencionales hasta por 2 semanas, en lugar del almacenamiento ultrafrío requerido anteriormente, lo cuál podría mejorar su distribución (ver comunicado).
Un debate derivado de la vacunación es su eficacia. En un primer momento, los datos presentados por las farmacéuticas causaban recelo al no haberse publicado con estudios científicos en algunos casos, y además, esa eficacia se ha medido en un periodo de pocos meses, por lo que hay gente que sugiere que habría que estar atentos porque puede caer su eficacia a la mitad en medio año. Un estudio confirmó que las vacunas de Pfizer y Moderna generaban anticuerpos similares entre sí, y similares a los que se producen en las personas infectadas (ver estudio), si bien ponía de relieve una menor capacidad neutralizante ante las nuevas variantes detectadas desde diciembre de 2020. En febrero de 2021, un estudio encontró que los anticuerpos de las personas vacunadas con la vacuna de Pfizer fueron moderadamente efectivos contra el virus original después de su primera dosis de vacuna, menos efectivos contra la variante británica (Kent) y no pudieron neutralizar la variante sudafricana. Sin embargo, tuvieron fuertes respuestas de células T contra todas las variantes conocidas después del primer pinchazo, por lo que se pensaba que puede que no proteja necesariamente contra la infección, pero es muy probable que esta primera dosis facilite mucho que su sistema inmunológico dé una buena respuesta la próxima vez. La segunda dosis se cree que produce una respuesta de anticuerpos robusta y buena, porque las células T ya están allí, listas para reaccionar (ver estudio).
En marzo se publicaba un estudio realizado en pacientes vacunados entre el 20 de diciembre de 2020 y el 1 de febrero de 2021, sobre la efectividad de la vacuna de Pfizer. Las conclusiones fueron las siguientes, en cuanto a las efectividades estimadas de la vacuna para los resultados del estudio en los días 14 a 20 después de la primera dosis, y a los 7 o más días después de la segunda dosis (ver estudio):
- Para infección documentada, 46% y 92%, respectivamente
- Para Covid-19 sintomático, 57% y 94%, respectivamente
- Para hospitalización, 74% y 87%, respectivamente
- Para la enfermedad grave, 62% y 92%, respectivamente
- Para prevenir la muerte por Covid-19 fue del 72% durante los días 14 a 20 después de la primera dosis.
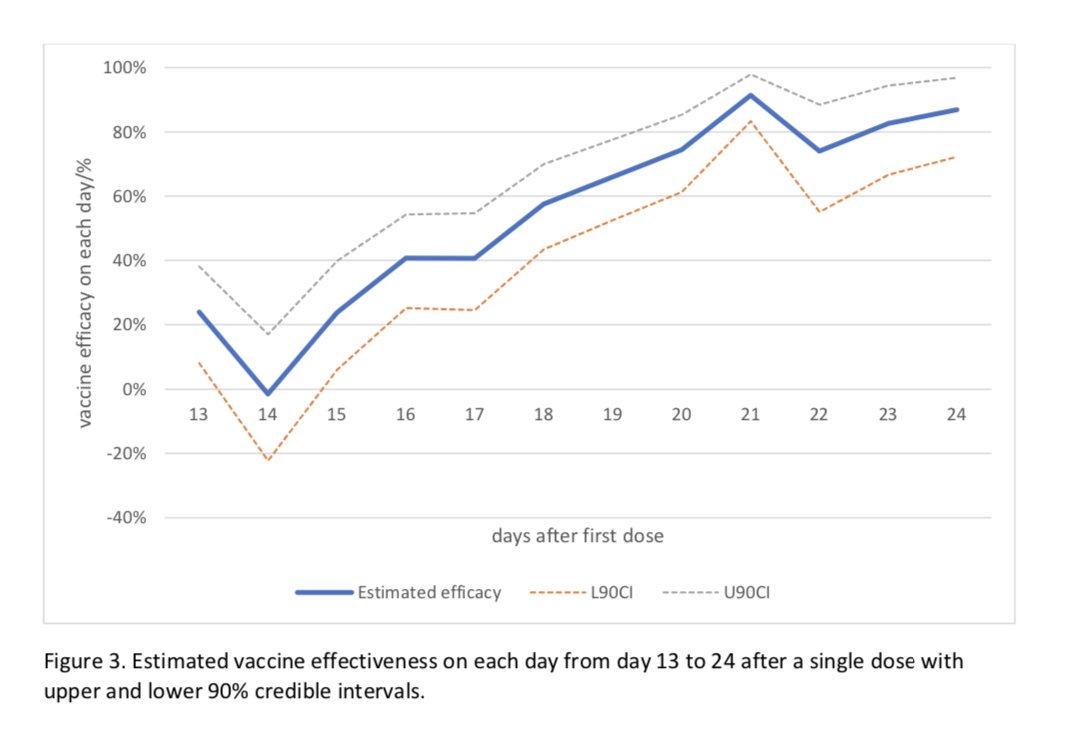
Un estudio en más de 23.000 personas en Reino Unido, publicado en The Lancet (ver estudio), mostraba que la vacuna BNT162b2 (Pfizer) puede prevenir la infección sintomática y asintomática en adultos en edad laboral. Esta cohorte fue vacunada cuando la variante dominante en circulación era B.1.1.7 y muestra efectividad contra esta variante. Una sola dosis de la vacuna BNT162b2 mostró una efectividad de la vacuna del 70% (IC del 95%: 55–85) 21 días después de la primera dosis y del 85% (74–96) 7 días después de dos dosis en la población de estudio.
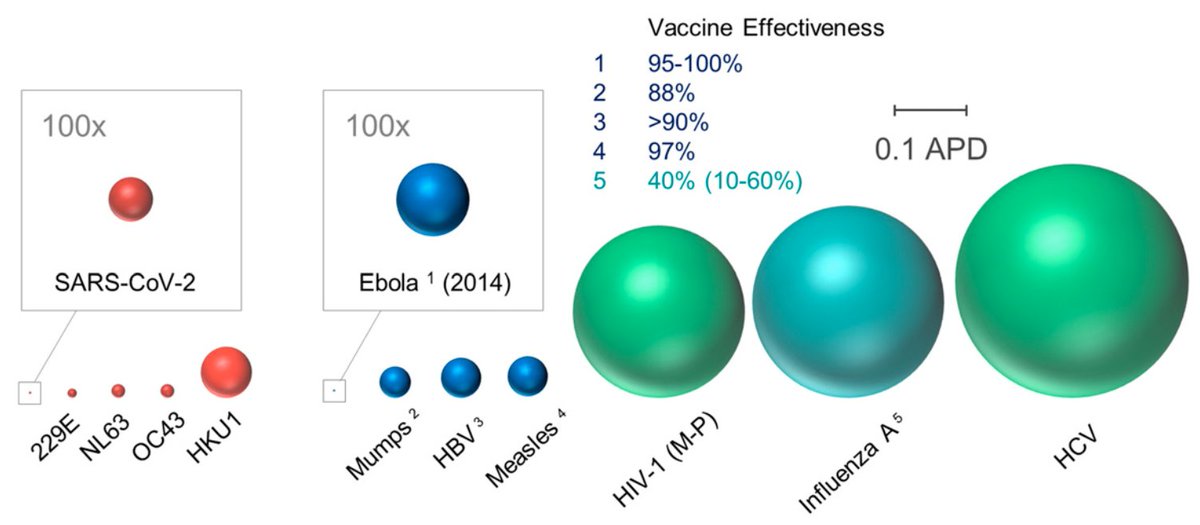
También es importante tener en cuenta que la comparación de la eficacia de las vacunas no es fiable, porque parten de ensayos clínicos diferentes, y algunas se ensayaron en momentos más tardíos con más incidencia, y otras variantes nuevas en circulación, y además, pueden influir otros factores, ya que, genéticamente, las poblaciones utilizadas por los ensayos pueden diferir, y por tanto, puede haber variaciones en su susceptibilidad. En la siguiente gráfica puedes ver la diferencia de ensayos en EEUU en cuanto a las vacunas de Pfizer, Moderna y Janssen, y los realizados por Janssen (Johnson & Johnson) en Brasil y Sudáfrica. Se puede observar que las vacunas de Moderna y Pfizer/BioNTech que presentaron una eficacia del 94 y 95 % respectivamente, se evaluaron en individuos infectados con el SARS-CoV-2 inicial, en Estados Unidos, en un periodo relativamente bajo en el índice de casos. Por el contrario, la de Janssen, con una eficacia del 72 %, se ensayó en Brasil y Sudáfrica, en cuyos países se presentaron dos variantes nuevas (más infecciosas) y en periodos bajos, moderados y altos de infección.
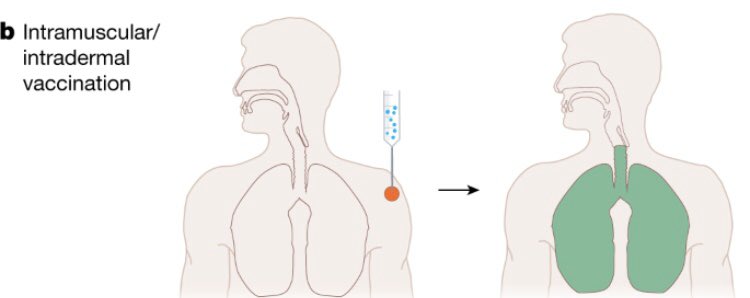
Otro aspecto interesante, según José Jiménez, investigador sobre virus emergentes en el Departamento de Enfermedades infecciosas del King’s College de Londres, es el hecho de que las primeras vacunas podrían ofrecer una inmunidad funcional, es decir, ayudarían a evitar síntomas, pero no está claro si evitarían una infección, y por tanto, que se pueda contagiar a otros, principalmente por la vía de administración de la vacuna que se va a utilizar en estas vacunas. En una infección natural de tipo respiratorio, el virus entra por las vías respiratorias altas, lo que provoca la formación de anticuerpos de tipo IgA, y es más tarde, cuando pasa a las vías respiratorias bajas, cuando el organismo produce anticuerpos IgG. Por eso después de una primera infección hay cierta protección.
Las vacunas intramusculares o intradérmicas de Pfizer o Moderna van a provocar que el organismo produzca principalmente anticuerpos IgG, que son los que van a proteger en las vías respiratorias bajas (pulmones). Esto podría dar lugar a que la persona vacunada se pudiera infectar, y por ello, el virus podría multiplicarse libremente en las vías altas, lo que podría otorgar a la persona vacunada el potencial de poder contagiar a terceras personas. Es decir, la persona vacunada tendría una inmunidad funcional (puede infectarse y ser contagioso, pero con menos síntomas).
Sin embargo, habría quizás que perseguir una inmunidad esterilizante, que es aquella en la que se consigue evitar la infección, y por lo tanto, la transmisión y la enfermedad. Una forma de solventar esto podría ser mediante el uso de vacunas que se administren intranasalmente, de las cuales hay varias en desarrollo, y de las que se espera que puedan tener este efecto.
No obstante todo esto, un estudio sobre la vacuna de Moderna (mRNA-1273) en primates no humanos, concluyó, además de que había niveles de anticuerpos superiores tras su administración a los de un suero en fase de convalecencia en humanos, que la replicación viral no fue detectable en las vías respiratorias de los mismos (ver estudio). Además, la evolución en febrero de 2021 de la campaña de vacunación en Israel (país puntero en la administración de la vacuna de Pfizer) sugieren que reduce significativamente la carga viral, por lo que esto podría tener un efecto fundamental a la hora de limitar la transmisión (ver noticia).
Conforme han ido avanzando los meses tras la vacunación, en efecto, se han ido conociendo casos de infecciones de personas que habían recibido una dosis o pauta completa de la vacuna, si bien en general habían sido casos de infecciones leves o moderadas. Por ejemplo, en España, una profesora vacunada con Astra Zeneca se contagió mes y medio después, y su hija sufrió una reinfección (ver noticia). En algunas residencias de mayores hubo caso de contagios en mayores vacunados previamente con Pfizer (ver noticia).
También se confirmó que las personas completamente vacunadas podrían contraer variantes del COVID y podrían ser transmisores potenciales. Investigadores de la Universidad de Washington secuenciaron muestras de 20 trabajadores de la salud que contrajeron el virusd después de recibir ambas dosis de Pfizer o Moderna. Los 20 estaban infectados con variantes de preocupación o VOCs: ocho tenían la variante inglesa, uno la sudafricana, diez alguna variante de California y otro la brasileña. Tras comparar las muestras con otras de más de 5.000 personas no vacunadas con COVID, se observó solo el 33% de los no vacunados tenía infección por una VOC, frente al 100% de vacunados. Sin embargo, en el caso de los vacunados, se encontraron cargas virales elevadas, por lo que podrían tener capacidad de transmitirlo, si bien no se sabe si transmitieron la enfermedad a otros, y ninguno tuvo que ser hospitalizado. A 30 de abril se habían documentado en EEUU 10.262 casos de infección en vacunados, entre los 101 millones de personas totalmente vacunadas (0'01%), correspondiendo un 65% a variantes VOC entre las secuenciadas (ver artículo).
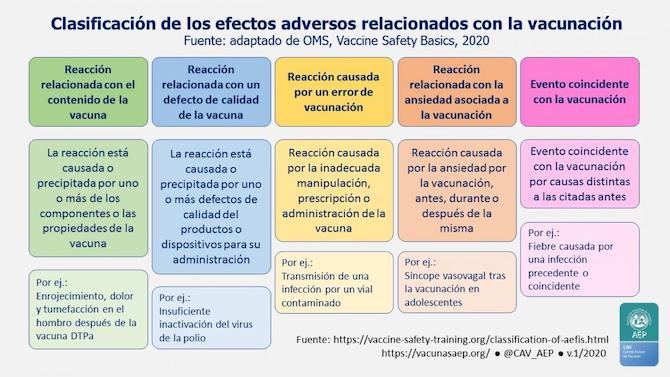
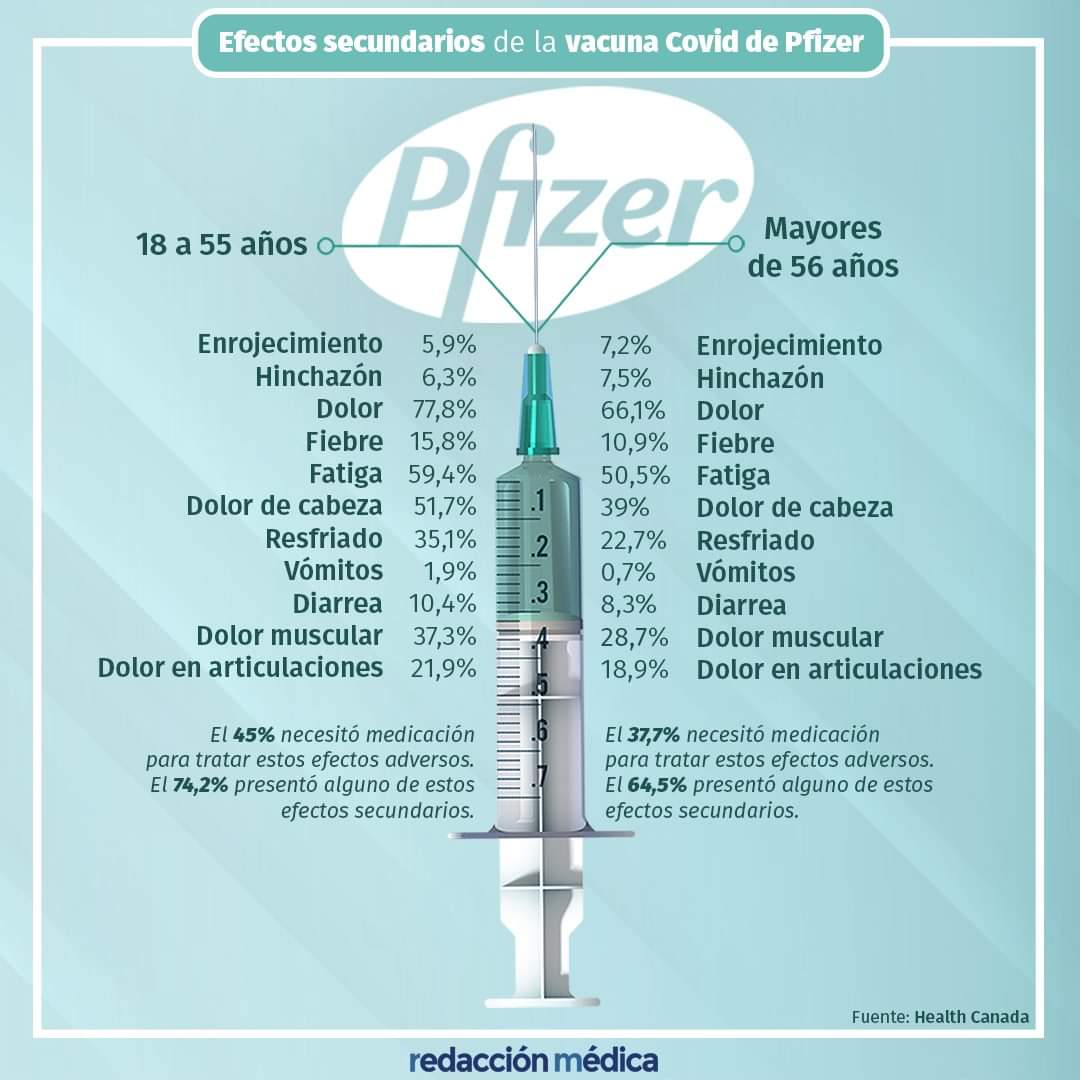
Cómo no, otro interrogante son los posibles efectos secundarios. Cuando empezó a administrarse la vacuna de Pfizer en diciembre de 2020, se documentaron algunas reacciones adversas. En el siguiente cuadro se pretende ilustrar algunos de los efectos secundarios más comunes a esta vacuna. Algunas noticias comenzaron a describir efectos secundarios, en algunos casos, magnificados según los expertos, como el de una enfermera que se desmayó tras administrársela en EEUU (ver noticia). En España muchas personas han experimentado efectos como fuerte dolor en el brazo, febrícula, escalofríos o dolor muscular.
Con respecto a los efectos secundarios de la segunda dosis, según una app del King’s College disponible en el Reino Unido (Zoe app, https://covid.joinzoe.com) y tras 10.000 respuestas de vacunados hasta el mes de febrero de 2021, el 45% reportaba efectos locales como dolor e hinchazón en el lugar de la segunda inyección. Un 22% presentaban sintomatología sistémica (en todo el cuerpo) como escalofríos, febrícula y dolores y que se resuelven en unos muy pocos días. También se han documentado adenopatías axilares como efecto secundario, que acaban desapareciendo a los pocos días (ver artículo).
Se comprobó que los efectos sistémicos son más frecuentes en los que se expusieron previamente al virus, ya que un tercio de ellos tuvieron síntomas, frente a un 20% de los vacunados que no habían sufrido infección previa. Los síntomas se deberían a que hubo un efecto positivo de la primera dosis y ya se ha generado una respuesta primaria contra el antígeno viral. Tras la segunda dosis, la reacción inflamatoria se produce, y se inicia la respuesta secundaria, lo cual es una buena señal. La fiebre, el dolor y la inflamación la produce la respuesta inmunitaria y es buena para combatir la infección. No obstante, la ausencia de reacción tampoco significa que la vacuna no esté siendo efectiva, ya que cada persona reacciona de manera distinta.
Otro de los debates surgidos con respecto al desarrollo de la vacuna gira en torno a la seguridad de las nuevas vacunas basadas en ARN mensajero. Según Shane Crotty, científico experto en vacunas e inmunología, en cada momento una célula humana tiene más de 5000 "mensajes" de ARN, que son temporales y descartados por las células en cuestión de minutos u horas tras ser leídos (es decir, el ARN mensajero inyectado en una vacuna no formará parte de nuestro cuerpo de manera permanente). Estos mensajes temporales de las vacunas instruirán a la célula para fabricar una única proteína del virus (en este caso, la proteína S), por lo que es imposible que el ARN inyectado pueda fabricar unidades del virus, que contiene bastantes más proteínas. Además, a finales de noviembre se habían suministrado sobre 70.000 dosis de este tipo de vacunas, y los informes independientes (no controlados por las compañías farmacéuticas) no habían reportado ningún dato preocupante, si bien no hay que descartar que su administración no provoque algún efecto secundario pasajero, lo cuál incluso podría ser una buena señal, pues el sistema inmune tiende a "recordar" aquellas cosas que hacen daño.
También han surgido dudas acerca de la posibilidad de que el ARN mensajero inoculado pudiera integrarse en el ADN de las células humanas. Dado que el ARN mensajero se degrada con facilidad, el tiempo que puede estar en las células es demasiado corto como para pensar que podría "hacer otras cosas" distintas a la traducción de la proteína S del virus. En principio, este ARN entrará en la célula mediante endocitosis, y quedará en el citoplasma, que es donde se encuentran los ribosomas que deberán utilizarlo para sintetizar la proteína S, mientras que la cromatina que contiene el ADN está en el núcleo de la célula, separado del citoplasma de la misma. Si bien hay ciertos ARN que pueden entrar al núcleo celular (por ejemplo, el ARN del virus de la gripe), no parece posible en este caso, pues para ello deben contener una información genética determinada. Además, no es fácil que un ARNm pueda integrarse dentro de una secuencia de ADN, pues previamente el ARN debería convertirse en otra secuencia de ADN mediante la acción de una enzima denominada transcriptasa inversa, que se encuentra en retrovirus como el del VIH. Estas ezimas son muy específicas y requieren de unas condiciones determinadas para poder funcionar (ver explicación de cómo funcionan). Además, cualquier ARN que se encuentre con una transcriptasa reversa no tiene por qué convertirse en ADN, y se dice que si el ARN de la vacuna se encontrase con nuestro genoma no podría llegar a integrarse (ver artículo). En el siguiente cuadro puedes ver una comparativa entre las vacunas de ARNm de Pfizer y Moderna, elaborado por Sonia Villapol.
Otra problemática de las vacunas podría ser su distribución a lo largo de todo el planeta. Algunas voces autorizadas alertaban en diciembre de 2020 de que casi un cuarto de la población mundial no podría tener acceso a una vacuna hasta 2022, además de que en ese mismo mes, el 51% de las dosis estarían destinadas a países de rentas altas, que tan solo representan el 14% de la población mundial, lo que pone de relieve las desigualdades a la hora del acceso a la vacuna (ver artículo). No obstante, países como España prevén poder donar dosis a países más necesitados de África o América Latina (ver noticia). También llama la atención que ya durante los primeros días de vacunación se podían ver "ofertas" para comprar dosis de la vacuna en la dark web (ver noticia), que es parte del contenido de internet no accesible fácilmente mediante navegadores y buscadores, que muchas veces se usa con fines oscuros.
Con respecto a las personas que ya superaron la infección, expertos también recomiendan su vacunación, principalmente porque los diferentes sistemas inmunológicos han respondido de manera muy diferente al virus, señalando algunos que si bien el 90% han generado una respuesta inmune duradera de hasta ocho meses, otro 10% parecía no tener una buena respuesta inmunológica tras este mismo periodo de tiempo, como podrían confirmar los casos de reinfección documentados. De esta forma, aquellas personas cuyos sistemas inmunológicos no produjeron una respuesta sólida podrían alcanzar mediante la vacunación a las que sí lo hicieron, pues parece haber menos variabilidad en las respuestas inmunitarias de las personas a las vacunas que a la infección natural. El 30 de enero de 2021, un estudio publicado indicaba que, tras estudiar las respuestas de anticuerpos a una sola dosis de las vacunas Pfizer-BioNTech o Moderna en sanitarios con infección previa confirmada, y compararlas con las respuestas de anticuerpos de sanitarios que con test de IgG negativo, se detectó que el personal sanitario que había superado la infección mostró claras respuestas secundarias de anticuerpos a la vacunación que aumentaron rápidamente a los 7 días y alcanzaron su punto máximo a los 10 y 14 días después de la vacunación. En todos los momentos de tiempo analizados, los sanitarios con infección previa mostraron títulos de anticuerpos significativamente más altos en comparación con los trabajadores sanitarios sin infección previa. Por ello, los hallazgos sugerían que una dosis única de vacuna para pacientes que ya han tenido COVID-19 confirmado podría ser una buena estrategia en época de escasez de vacunas (ver estudio).
En los primeros compases de vacunación, con la vacuna de Pfizer, algunos países sopesaron la posibilidad de cambiar los plazos entre dosis. En el Reino Unido cambió la estrategia dilatando la inoculación de la segunda dosis hasta 12 semanas (ver noticia). La Agencia Europea del Medicamento, el 5 de enero de 2021, recomendaba no retrasar la segunda dosis de la vacuna de Pfizer más de 42 días (ver noticia). Al no ser estas las condiciones de los ensayos previos a la aprobación de la vacuna, la medida fue muy polémica y generó un amplio debate entre la comunidad científica, con detractores de estos retrasos. A favor de esta decisión estaría el hecho de que la eficacia de la vacuna de Pfizer-BioNTech es del 52% tras la primera dosis, y del 95% después de una segunda dosis a las tres semanas, lo cual podría decelerar el notable crecimiento de contagios que estaban sucediéndose en diciembre y enero (ver estudio). Hay virólogos que temen que alargar el intervalo de dosificación de 3 semanas a 3 meses, podría acelerar la aparición de mutaciones al crear un grupo de personas que tienen suficientes anticuerpos para ralentizar el virus y evitar el desarrollo de síntomas, pero no lo suficiente para eliminarlo. Esas personas podrían incubar virus con mutaciones que les permitan esquivar los anticuerpos inducidos por la vacuna. E incluso debido a que la mayoría de las vacunas COVID-19 generan inmunidad a una sola proteína, la proteína S en la superficie del virus, las nuevas vacunas podrían ser más fáciles de evadir para los virus mutantes que otras vacunas que evocan una inmunidad más amplia (ver artículo). Sin embargo, otros especialistas, como Michael Mina, opinan que, las personas no vacunadas, también tienen la llamada "inmunidad parcial" mientras están infectadas. Al considerar el escape de la inmunidad derivada de la proteína S, hay que considerar que todos los individuos sin inmunidad esterilizante están en riesgo de inducir un mutante tras una infección, ya que bien por infección, o bien por una única dosis de la vacuna, las personas crearán anticuerpos contra la proteína S. Además, una persona vacunada tendrá anticuerpos previos que pueden responder antes a la replicación del virus en una infección, lo que limitaría las opciones de que el virus mute, en comparación con una persona sin anticuerpos. Por lo que no está tan claro que esto pudiera suceder, y siempre lo mejor será prevenir los contagios (ver Twitter). Más tarde, en febrero de 2021, tras comprobar cómo iba la evolución de la campaña de vacunación en Israel (país que comenzó su campaña de vacunación a un alto ritmo), se demostró que una sola dosis de vacuna es altamente protectora, aunque puede llevar hasta 21 días lograrlo (ver estudio).
Otro debate que surgió en plena etapa de vacunación, en algunos casos, es el de la posibilidad de cambiar las dosis a administrar. Así, por ejemplo, un ensayo clínico fase II sugería que la administración de la mitad de dosis de la vacuna Moderna (50 μg en vez de 100 μg) podría resultar en una eficacia similar a la dosis completa (ver artículo).
La celeridad con que se desarrollaron las vacunas de ARN mensajero de Pfizer y Moderna se debe, según parece, al riesgo que tomaron investigadores chinos en enero. La vacuna de Moderna según parece se desarrolló en pocos días, durante un fin de semana, una vez que se dispuso de la secuencia genética del virus el 10 de enero de 1010. Esta secuencia se publicó diez días antes de que China reconociera abiertamente la gravedad de la enfermedad, al admitir la transmisión entre humanos, y cerrar la ciudad de Wuhan, epicentro de la pandemia, y también mientras la OMS todavía restaba importancia a lo sucedido. Esta secuencia se publicó en un depósito de código abierto por el profesor del Centro Clínico de Salud Pública de Shanghai y la Escuela de Salud Pública Yong-Zhen Zhang, quien había recibido el virus el día 3 de enero. Durante casi dos días de trabajo concienzudo, habían logrado secuenciar el genoma del patógeno, y compartió el genoma con otros investigadores, entre ellos, un científico australiano, Eddie Holmes, quien el día 11 de enero llamó a Zhang para pedir permiso y liberar el genoma al mundo, accesible en esta dirección web: https://virological.org/t/novel-2019-coronavirus-genome/319. De este modo, los científicos de todo el mundo se pusieron a trabajar rápidamente, y se consiguieron realizar las primeras vacunas de ARN mensajero, que solo necesitan la secuencia del día, en poco tiempo.
- El conocimiento de virus previos similares (SARS-CoV-1 y MERS-CoV principalmente)
- El uso de prototipos de vacunas preexistentes
- El solapamiento de fases clínicas
- Fabricación con riesgo de pérdidas antes de terminar estudios
- Inversión económica sin precedentes
A pesar de los esfuerzos a nivel mundial, hay expertos que son más optimistas y otros más pesimistas, pues a día de hoy, no se ha conseguido una vacuna efectiva contra los seis coronavirus anteriormente descubiertos (ver noticia). También se ha publicado en prensa que varios desarrolladores estarían buscando una inmunidad legal ante posibles efectos adversos (ver noticia). Con respecto a los posibles efectos secundarios que pudieran tener las vacunas desarrolladas, expertos dicen que no se esperan efectos adversos graves, pero sí son posibles algunos leves o de grado medio (ver artículo). Durante la fase 3 de algunas vacunas, se han descubierto algunos efectos secundarios, como por ejemplo:
- El 8 de septiembre, AstraZeneca anuncia que paralizaba la fase 3 de pruebas, ante un posible caso de reacción adversa que habría originado a un participante una mielitis transversa (ver noticia). Esto es normal en el desarrollo de vacunas. El día 12 del mismo mes se anunciaba la reanudación de pruebas. Y a mediados de octubre se supo que un voluntario había fallecido, aunque no había recibido la vacuna, sino un placebo (ver noticia).
- El ensayo de la vacuna JNJ-78436735 de Johnson & Johnson se detuvo el lunes 12 de octubre tras darse una enfermedad inexplicable en un voluntario. En principio, no se sabía si la enfermedad identificada tenía relación con la vacuna, pero los protocolos clínicos requieren que se realice una pausa mientras se investigaba (ver noticia).
Como dato curioso, se está estudiando también el papel protector que pueden tener determinadas vacunas ya existentes y comercializadas contra el SARS-CoV-2, a raíz de un estudio que sugería que la vacuna contra la tuberculosis (BCG) frenaba la gravedad de los pacientes, dado que los casos más graves se estaban dando en países en los que no existe una vacunación de la población contra la tuberculosis (ver noticia). También se ha especulado con el papel protector de otras vacunas, como por ejemplo la de difteria-tétanos-tos ferina (ver noticia), aunque luego se matizó desde algunas fuentes que no había pruebas de esto (ver noticia), o la del sarampión (ver noticia).
En este enlace del Washington Post puedes ver información actualizada de cuántas vacunas se encuentran en cada fase.
También puedes usar esta web, llamada covid-19vaccinetracker, con información detallada de todas las vacunas en desarrollo.

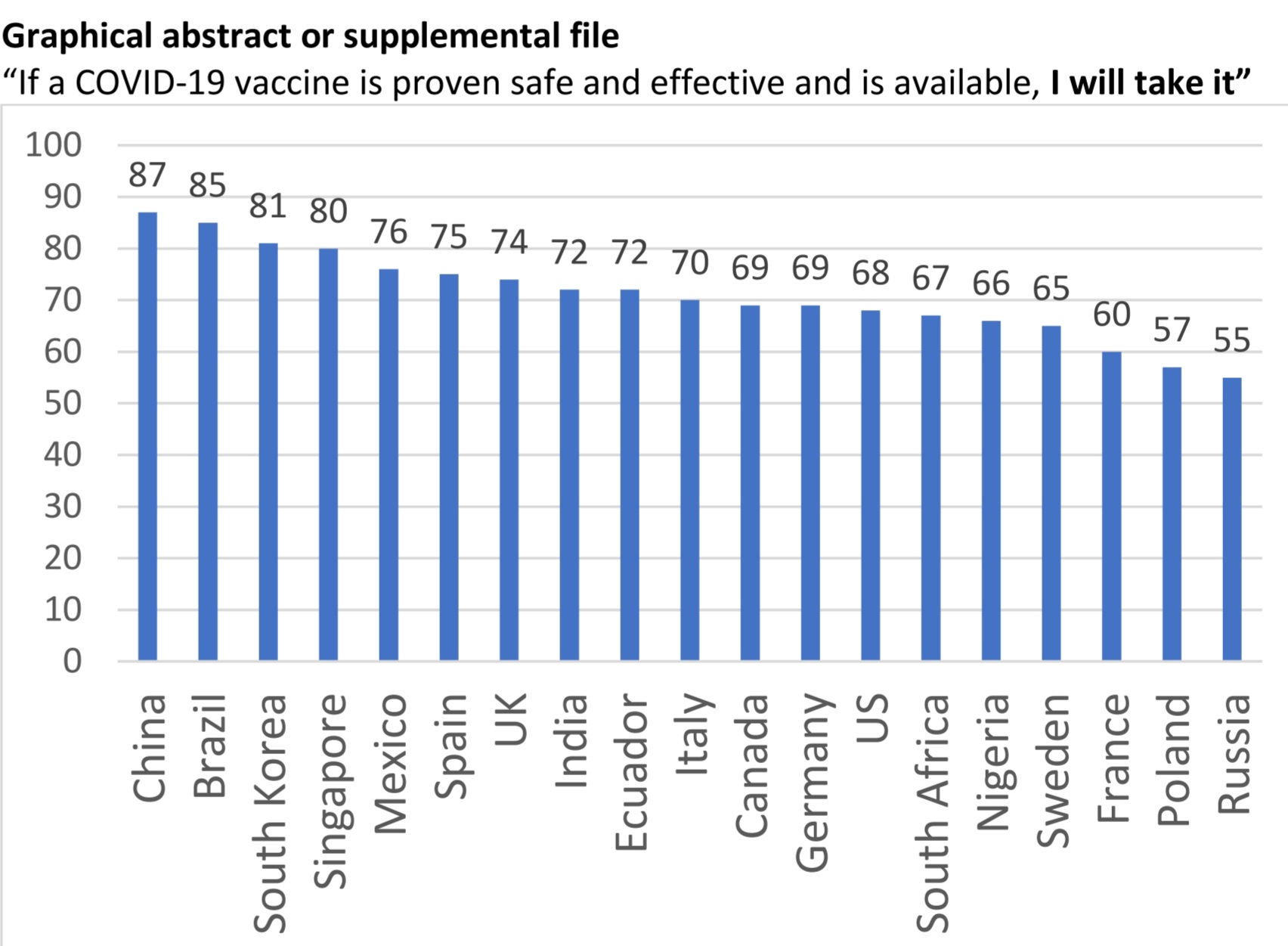
Otro punto a tener en cuenta es la aceptación que podría tener una campaña de vacunación. Además de los 'antivacunas', existen personas que en principio no ven con malos ojos vacunarse, pero sí que son escépticos ante una vacuna nueva, y prefieren esperar un tiempo por si esta pudiera tener efectos secundarios a corto/medio plazo. Un estudio piublicado en medxriv muestra cómo varía la aceptación de una eventual vacuna que funcionara es distinta en según qué países.
Fuente: medxriv
Hay expertos que opinan que la efectividad de las vacunas en desarrollo no serán tan efectivas como las de otras enfermedades, sino que sus efectos pueden ser más bien parecidos a las vacunas de la gripe, con una eficacia menor. Otros sin embargo opinan que, dada la baja variabilidad genética del SARS-CoV-2, más sencillo en teoría puede resultar encontrar una vacuna eficaz. En el siguiente gráfico se representa la variabilidad de distintos virus, siendo más variables las esferas de mayor tamaño.
En noviembre, el gobierno danés anunció el sacrificio de miles de visones, pues se detectó en estos animales una mutación del virus que podía comprometer las vacunas ya en avanzada fase de desarrollo. Al parecer, esta variante que también se había detectado en humanos, no se veía afectada por los anticuerpos producidos por pacientes recuperados de COVID (ver noticia).

Fuente: The guardian
Como curiosidad, se espera que la mayoría de vacunas desarrolladas sean intramusculares, y por ello, solo producirán IgG, que son los anticuerpos que genera nuestro organismo como respuesta inmunitaria ante infecciones de vías respiratorias inferiores, pero no favorecerán el desarrollo de anticuerpos IgA, que son los que genera nuestro organismo como respuesta a las infecciones de vías respiratorias superiores (ver estudio sobre vacunas en desarrollo).
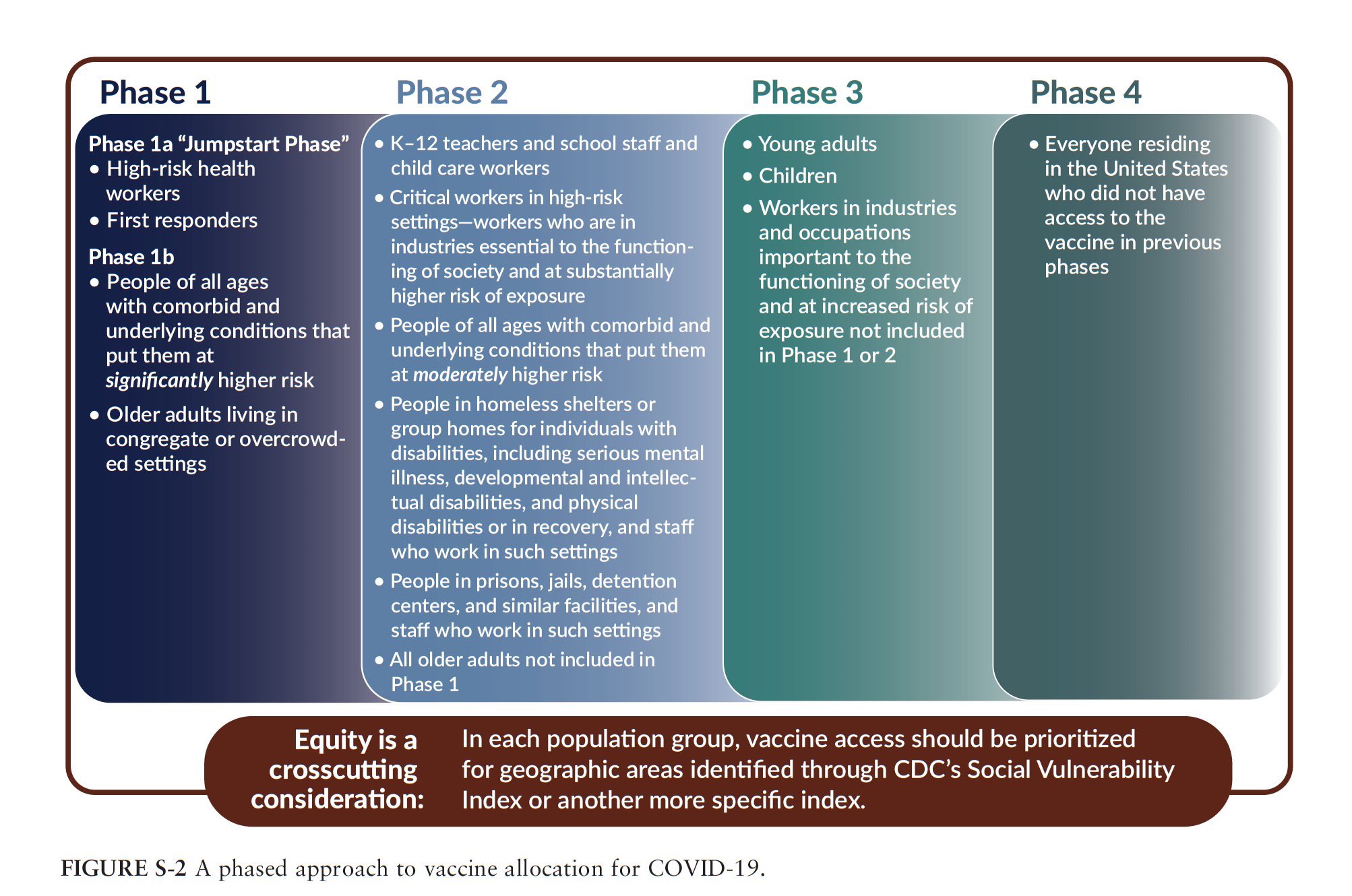
Las vacunas tendrán que administrarse en distintas fases. La CDC americana publicó en noviembre una posible planificación de fases de vacunación, empezando por las personas con más riesgo y más expuestas, hasta acabar por la población que menos riesgo podría tener.
En esta gráfica puedes ver la comparativa de financiación de algunas de las vacunas en desarrollo.
PLAN DE VACUNACIÓN EN ESPAÑA
En España se van a llevar fases de vacunación, donde tendrán prioridad grupos de más riesgo, como puedes ver en la siguiente infografía:

Las perspectivas iniciales eran estas:
- La vacuna de Pfizer fue aprobada en diciembre de 2020 por la Agencia Europea del Medicamento, y se compraron unos 300 millones de dosis. La compañía suministraría a la Unión Europea unas 3.500.000 por semana dosis hasta marzo (son necesarias dos dosis por persona), si bien este suministro podría aumentar. No obstante, en enero, la compañía empezó a anunciar que tendría que recortar el suministro. Inicialmente se ponían 5 vacunas por vial, pero posteriormente, con el uso de material adecuado, se autorizó la extracción de una sexta dosis (ver información aquí).
- La vacuna de Moderna, aprobada en Europa en enero de 2021, suministraría un total de 160 millones de vacunas, de las cuales España recibiría 8 millones, aunque no se esperaba recibir muchas de ellas hasta marzo (quizas hasta 2 millones).
- La vacuna de Oxford-AstraZeneca, aprobada en Europa en enero de 2021, tras su aprobación el 30 de diciembre de 2020 en Reino Unido, suministraría 400 millones de dosis. En un escenario ideal, podrían llegar hasta 5 millones de dosis antes de abril a nuestro país. En enero sin embargo, se anunciaron limitaciones en la producción (ver noticia).
- La vacuna de Janssen (Johnson % Johnson), suministrará a la Unión Europea otros 400 millones de dosis. Posiblemente aprobada en Europa en febrero de 2021, y se podría vacunar a otros dos millones de personas en el primer trimestre del año con esta vacuna monodosis.
- Otras vacunas que podrían llegar más adelante son las de CureVac y Sanofi
- Con estas perspectivas, se podría vacunar total o parcialmente hasta a 7 millones de españoles (15% de la población), incluyendo a personas mayores y sanitarios.
- Tras ello, a finales de marzo o abril, podría llegar la vacuna de Novavax, y tambén la de CuraVac
- Si todo va bien, al finalizar abril podría haber 10 millones de vacunados, al finalizar mayo unos 15 millones, y a finales de junio un 50% de la población (unos 23 millones), lo que incluiría los grupos con más mortalidad, como sanitarios, mayores, trabajadores esenciales, personas con patologías graves...
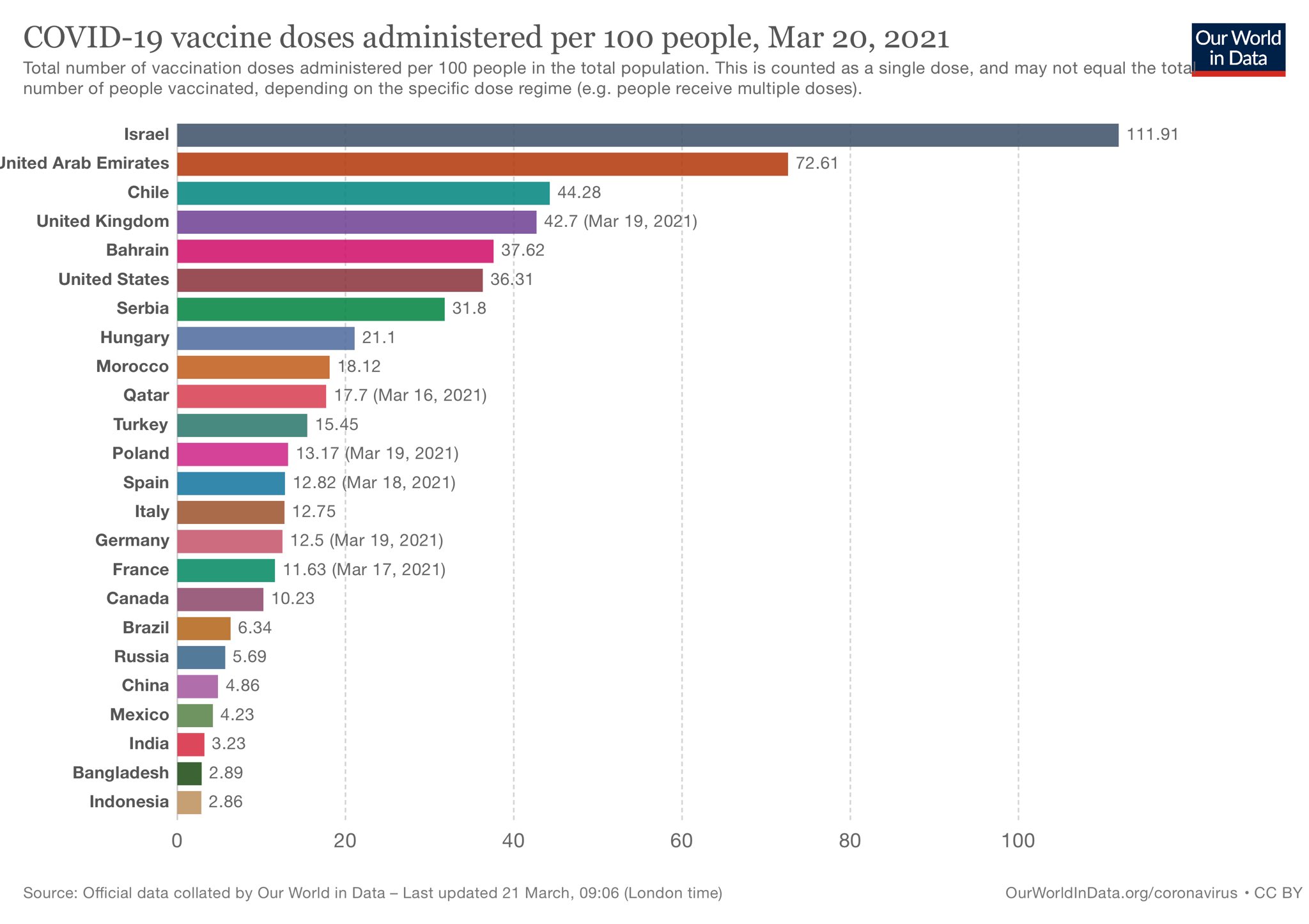
Más adelante, las cosas fueron cambiando: hubo retrasos en las entregas, se paralizó una semana la vacunación con Astra Zeneca por dudas sobre su seguridad (tal y como aconseja una fase de vigilancia farmacológica), etc. A finales de marzo de 2021, había varios países con un ritmo de vacunación significativamente mayor a España, como se puede apreciar en el siguiente gráfico.
Consulta aquí la estrategia de vacunación.
BENEFICIOS OBSERVADOS DURANTE EL PROCESO DE VACUNACIÓN
Uno de los beneficios más sorprendentes es que parece que están mejorando los síntomas de personas con COVID persistente (ver artículo).
PROBLEMAS OBSERVADOS DURANTE EL PROCESO DE VACUNACIÓN
Un problema preocupante fue la aparición de casos de trombos venosos cerebrales aparecidos con las vacunas de Astra Zeneca y Janssen, suponiendo esto la paralización de la vacunación con ambas en algún momento.
En el caso de Astra Zeneca, algunas muertes podrían estar relacionadas con la administración de la vacuna, como el caso de una profesora de Málaga (ver noticia) o el de un profesor de Toledo (ver noticia). Al parecer, esta vacuna podría causar un evento de trombosis venosa cerebral (denominada VITT, o trombocitopenia inmune trombótica inducida por vacuna, similar a los casos de trombocitopenia inducida por heparina o HIT). Se especuló con que algún componente de la vacuna (podría ser el EDTA, ácido etilendiaminotetraacético, conservante de la vacuna), actuaría rompiendo las uniones celulares de células endoteliales, con lo que entraría el adenovirus y sus proteínas en el torrente sanguíneo. Se generaría un estado proinflamatorio y, en determinadas personas, el inicio de una respuesta mediada por anticuerpos que acaba provocando el desarrollo de anticuerpos anti PF-4 (factor plaquetario 4, proteína que está en la membrana de las plaquetas), que son los que acaban generando la trombocitopenia, al aglutinar las plaquetas formando trombos (ver estudio).
En el caso de Janssen, el riesgo de coágulos raros parecía claramente depender del sexo y la edad (7 por millón en mujeres de 18 a 49 años frente a 0,9 por millón en mujeres mayores de 50 años y ninguno en hombres, aunque se están revisando casos adicionales).
Afinando un poco más, parecía más alto en mujeres de 30 a 39 años (11,8 por millón, en comparación con 0 por millón para mujeres de 65 años o más).
Otra preocupación relacionada con la vacuna de Pfizer fue la aparición de problemas cardíacos (miocarditis) en hombres menores de 30, habiéndose registrado hasta 32 casos pocos días después de la vacunación (ver artículo).
El periodista científico Kai Kupferschmidt afirmaba en twitter, que, a partir de datos obtenidos de la Agencia Europea del Medicamento, los casos reportados de trombosis con trombocitopenia en la Unión Europea eran, a fecha 21 de abril, los siguientes (ver tweet):
VACUNAS DE ARN MENSAJERO
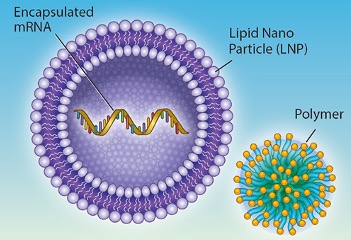
Las vacunas de ARN mensajero (ARNm) funcionan inyectando fragmentos de ARN similares a una parte del ARN original del virus. Estos fragmentos tienen el código necesario para fabricar las proteínas de la estructura del virus. El objetivo de estas vacunas es que este ARNm sea "leído" por unos orgánulos del interior de la célula, llamados ribosomas, que se encuentran adosados a otro orgánulo que recubre el núcleo celular, llamado retículo endoplasmático rugoso, para fabricar proteínas del virus. Los ribosomas encargan de ir leyendo el código del ARNm, lo traducen, y generan una secuencia de unas moléculas denominadas aminoácidos, que posteriormente se repliegan en una estructura espacial mediante enlaces atómicos, formando la proteína. Las vacunas de Pfizer y Moderna utilizan este sistema, para que nuestro organismo genere la proteína S (espiga) del virus (no todo el virus), de forma que luego pueda ser reconocida por nuestro sistema inmune y pueda fabricar anticuerpos neutralizantes contra esa proteína, similares a los que se generan cuando hay una infección real. De esta forma, ante una eventual infección, nuestro organismo tendría ya anticuerpos que le permitirían comenzar a defenderse de manera temprana.
Con respecto al ARNm de la vacuna de Pfizer (BNT162b2, Tozinameran o Comirnaty), un genial post de Bert Huber analizaba su secuencia genética (ver artículo). La vacuna de ARNm BNT162b tiene 4284 nucleótidos. La proteína S es una secuencia de unas moléculas orgánicas denominadas aminoácidos, que se van uniendo unas con otras, y se van eligiendo cuando se sintetiza en base a la secuencia de nucleótidos del ARN.

Fuente: OMS
Para comenzar la producción de la vacuna, alguien cargó este código en una impresora de ADN, que se encarga de producir moléculas de ADN reales a partir de esa secuencia de código.

Impresora DNA. Fuente: Novoengineering
Una vez que se ha conseguido "imprimir" ese ADN, se producen una serie de procesos bioquímicos para generar una secuencia de ARN equivalente en cierto modo, que es lo que acaba en la dosis de la vacuna: unos 30 microgramos de ARNm empaquetado en una cubierta lipídica. El ARNm empaquetado tiene el siguiente "esquema":

La secuencia empieza con los nucleótidos G-A (guanina y adenina), y tiene la misión de "marcar" el ARN para indicar que debe "traducirse" por los ribosomas (es decir, que debe usarse para la síntesis de proteínas). Posteriormente viene una secuencia (denominada 5'-UTR) que indica que es el inicio del ARN (extremo 5'), es decir, la zona donde debe empezar a leerse por parte del ribosoma para codificar la proteína, cuya lectura acabará en el otro extremo (3'). Esta región viene determinada por la siguiente secuencia de nucleótidos, en la que, como antes, G representa la base nitrogenada guanina, A representa nitrogenada adenina, C representa citosina, y en lugar de usar la cuarta base del ARN, uracilo (U), que forma uridina cuando se une a la ribosa del nucleótido, se emplea una base distinta, denominada por la letra Ψ, que representa una molécula denominada pseudouridina o 1-metil-3'-pseudouridilo:
GAAΨAAACΨAGΨAΨΨCΨΨCΨGGΨCCCCACAGACΨCAGAGAGAACCCGCCACC

Fuente: wikiwand
El 1-metil-3'-pseudouridilo se utiliza en lugar del Uracilo para evitar que nuestro cuerpo, a través del sistema inmune, destruya este ARN mensajero, al detectarlo como un agente extraño. Tras años de experimentación se descubrió que si el uracilo era reemplazado por esta molécula, nuestro sistema inmunológico se frenaría en su afán por destruirlo, y lo acabaría aceptando como algo natural.
Tras esto, hay una zona llamada péptido señal de la glicoproteína S (sig), que se encarga de señalizar que esta proteína que se va a sintetizar (la proteína S), debe salir de la célula desde los ribosomas del retículo endoplasmático rugoso. No es muy largo, pero es ligeramente distinto al del virus. Si se comparan ambos (poniendo U en el código de la vacuna para facilitar la comparación), se pueden observar que han cambiado algunas bases:

Los nucleótidos del ARNm se agrupan en grupos de 3 (esto se llama codón). En total, se pueden ver 16 codones, de los cuáles solo permanecen iguales 4 (el primero y los 3 últimos). En los restantes, hay un cambio o dos de bases. Sin embargo, a pesar de esos cambios, codifican los mismos aminoácidos, pues un aminoácido puede ser codificado por 2, 3 o hasta 4 codones distintos, como puedes ver en la siguiente tabla:

Así por ejemplo, el cuarto codón de esta secuencia, en el virus, es UUU, que codifica el aminoácido fenilalanina, y en la vacuna se sustituye por UUC, que sin embargo, codifica el mismo aminoácido. El objetivo de estos cambios era eliminar el mayor número posible de uracilos, así como aumentar el número de citosinas y guaninas (a veces a costa de adeninas) porque la conversión sería más eficiente.
A continuación, vendría el código de la proteína S en sí. ocupando 3.777 nucleótidos en los que se optimizaron los codones para minimizar el número de uracilos de manera similar a lo comentado anteriormente, excepto en una parte especial, en la que el cambio de bases de los codones supone el cambio de dos aminoácidos:

Como se ve en este trozo de secuencia, se han ido cambiando codones para sintetizar los mismos aminoácidos de la proteína, exceptuando dos posiciones consecutivas, donde cambian los codones AAA y GUU del virus, que codifican los aminoácidos K (lisina) y V (valina) respectivamente, por codones CCU que codifican el aminoácido P (prolina). Tras investigar, se observó también que estos dos cambios mejoraban enormemente la eficacia de la vacuna. Como nuestro organismo va a fabricar solo la proteína espiga del virus, y esta no se va a quedar fijada a una estructura, como sucede en el caso real del virus, donde se fija en la nucleocápside, la proteína fabricada por nuestro organismo adoptaría una estructura diferente, por lo que de quedar así, nuestro sistema inmune desarrollaría anticuerpos contra la proteína en esa conformación, pero no contra la proteína con la conformación que realmente tendría en el virus, por lo que no estaría protegiéndonos del mismo. Esta doble sustitución se describió en 2017 cuando se investigaban las proteínas espiga del SARS (SARS-CoV) y el MERS. Al ser la prolina un aminoácido muy rígido, actúa estabilizando la proteína en el estado que "se necesita mostrar" al sistema inmunológico. Otras vacunas también utilizan este sistema de doble prolina para estabilizar la proteína: Moderna, Janssen, Novavax y Pfizer. Sin embargo, no está contemplado por la vacuna de Astra Zeneca.
Síntesis de proteínas a partir de ARNm
Al final del código de la proteína, hay otra pequeña modificación. Al final de la síntesis, hace falta un codón de parada, para indicar al ribosoma que ha terminado de sintetizar la proteína. En el virus original, el codón es UAA (representado como s). En la vacuna se han usado dos codones UGA en su lugar:

Tras el código de la proteína, viene la región 3' del ARN (extremo 3'- UTR), que es una zona que no se "traduce" en la síntesis de la proteína. Se añadió una secuencia que confiere estabilidad al ARN. Y finalmente, la vacuna termina con una secuencia poliadenilada (es decir, con varias bases A), que es una protección contra la degradación; el ARNm se puede reutilizar muchas veces, pero cada vez que se usa, pierde alguno de los nucleótidos con adenina (A) al final. Cuando estas se agoten, el ARNm ya no será funcional y se descartará. Según estudios, el número óptimo de A al final en las vacunas de ARNm podría ser de hasta unos 120 aproximadamente. En el caso de la vacuna de Pfizer, acaba con 30 adeninas, luego un "enlazador" de 10 nucleótidos (GCAUAUGACU), y otras 70 adeninas.

Una vez analizado todo esto, podríamos ver que la secuencia original del virus, dentro de su ARN, para codificar la glucoproteína S espiga, que va de los nucleótidos 21563 a 25384, sería esta (fuente: Naukas):
AUGUUUGUUUUUCUUGUUUUAUUGCCACUAGUCUCUAGUCAGUGUGUUAAUCUUACAACCAGAACUCAAUUACCCCCUGCAUACACUAAUUCUUUCACA |
Todo este código, al agruparlo en grupos de tres nucleótidos (codones) codificarían una proteína con una secuencia de 1273 aminoácidos (se resaltan en azul los aminoácidos lisina K y valina V en las posiciones 986 y 987, que son los que cambiaron a prolina). Como puedes ver en la tabla que aparece a continuación, cada aminoácido está representado con una letra.
MFVFLVLLPLVSSQCVNLTTRTQLPPAYTNSFTRGVYYPDKVFRSSVLHSTQDLFLPFFSNVTWFHAIHVSGTNGTKRFDNPVLPFNDGVYFASTEKSN |
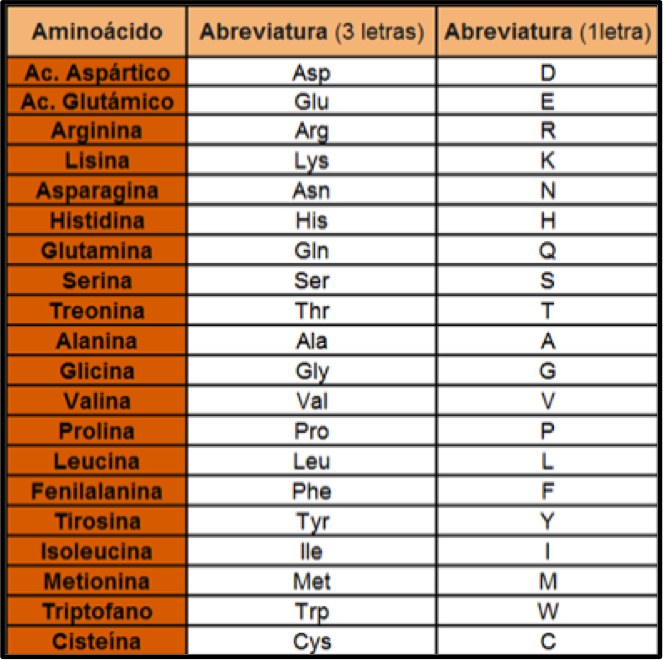
Fuente: g-se.com
La secuencia de ARNm sintetizada para la proteína S, haciendo los cambios en el uracilo, es la siguiente (en azul los dos codones modificados para cambiar los aminoácidos comentados por prolina):
AΨGΨΨΨGΨΨΨΨΨCΨΨGΨΨΨΨAΨΨGCCACΨAGΨCΨCΨAGΨCAGΨGΨGΨΨAAΨCΨΨACAACCAGAACΨCAAΨΨACCCCCΨGCAΨACACΨAAΨΨCΨΨΨCACA |
Y la secuencia completa de la vacuna se muestra a continuación, donde se destacan en verde las secuencias 5'-UTR y 3'-UTR, en rojo la secuencia que codifica el péptido señal, y los cambios de aminoácidos comentados en azul.
GAGAAΨAAAC ΨAGΨAΨΨCΨΨ CΨGGΨCCCCA CAGACΨCAGA GAGAACCCGC 50 |
Al final, entre el genoma original del ARN del virus y el de la vacuna, hay 1.061 nucleótidos cambiados, por lo que el porcentaje de identidad de las dos moléculas es del 72.24%. Sin embargo, la amplia mayoría de cambios en el ARN son silenciosos, y solo conducen al cambio de dos aminoácidos en la fabricación de la proteína, lo que hace que la proteína original del virus y la fabricada por el organismo en base al ARNm de la vacuna tengan una coincidencia del 99'84% de su secuencia de aminoácidos.
Como explica el inmunólogo José Gómez Rial en Twitter, una vez que se produce el pinchazo con la vacuna de ARNm, este atrae unas pocas células dendríticas, que son un tipo de células especializadas cuya función principal es procesar antígenos, de forma que lo llevan a su superficie y lo presentan a los linfocitos T, que son células más especializadas. Como el ARNm inoculado va dentro de una nanopartícula con cubierta lipídica, las células dendríticas no ven nada raro, así que estas esferas consiguen adentrar el ARNm en el interior de las células musculares del deltoides.
Al día siguiente del pinchazo, las células musculares comienzan a fabricar la proteína S a partir del ARNm, y comienzan a liberarla. Es en ese momento cuando las CD (células dendríticas) la captan, y corren al ganglio linfático axilar, al tiempo que avisan al resto de células dendríticas. En el ganglio, las CD presentan la proteína S a linfocitos T vírgenes (células en reposo que se encuentran en la fase G0 del ciclo celular, es decir, que no están en proceso de división). Es en ese momento cuando los linfocitos T reconocen la proteína S como algo extraño, y comienza la lenta activación de la respuesta inmune específica (la fabricación de anticuerpos). A la zona del pinchazo acuden más células dendríticas, y también neutrófilos, un tipo de glóbulos blancos que tienen la función de acudir al sitio de una infección para combatirla, y son los responsables de la inflamación local. Unos dos días después del pinchazo, apenas quedan restos del ARNm en el citoplasma de las células musculares, pues una vez que se sintetiza la proteína S a partir de ellos, unas enzimas, denominadas nucleasas, degradan el ARNm. Mientras, en el lugar del pinchazo, los mecanismos de autolimitación de la respuesta inmune se activan, al no detectar ninguna señal añadida de peligro, y los neutrófilos se retiran de la zona. Pero también siguen llegando al ganglio linfático axilar más CD con la proteína S (el antígeno) que se sigue produciendo en las células musculares. De esta forma, cada vez se activan más linfocitos T vírgenes que empiezan a transmitir la señal de activación a los linfocitos B vecinos. A los cuatro días, las células T activadas proliferan y siguen expandiendo su respuesta, de forma que pronto comenzará la especialización a linfocitos T efectores, que intervienen en la respuesta inmune liberando citoquinas o activando otras células. En otra zona del ganglio, las células B que ya han recibido la señal de activación, también proliferan y se expanden, y comienza la formación de los centros germinales en el ganglio, que son compartimentos anatómicos transitorios donde los linfocitos B maduros proliferan, se diferencian, y acaban produciendo los anticuerpos afines a la proteína de tipo IgM o IgG.
Un estudio sugiere que la primera dosis de las vacunas de ARNm estimulan la respuesta humoral (anticuerpos) y también la celular (linfocitos T CD4+).

Fuente: biorxiv
Otra vacuna cuyo desarrollo es más lento, y que utilizará ARNm, es la que está desarrollando en España el CSIC. Presenta diferencias significativas con otras vacunas de ARNm, como la de Pfizer o Moderna:
- El código de ARNm será más amplio, incluyendo más proteínas, no solo la proteína S. De esta forma se podrán crear anticuerpos contra otras proteínas del virus.
- El ARNm es autoamplificable, es decir, cuando entre en las células, podrá replicarse, y ser así leído más veces por los ribosomas, lo que conllevará una producción mayor de anticuerpos
- La idea es que la vacuna sea inhalada; de esta forma podría aportar protección en las vías respiratorias, que se consideran una puerta de entrada del virus, por lo que, a diferencia de las anteriores, podría prevenir incluso el contagio y por consiguiente la capacidad de contagiar a terceros, y no solo el desarrollo de enfermedad grave. Esto es lo que se conoce como inmunidad esterilizante.
VACUNAS DE VECTORES VIRALES CON ADN
El funcionamiento de estas vacunas es a partir de una cadena de ADN, que llegará al núcleo de la célula, donde tendrá lugar un proceso denominado "transcripción", que lo que hace es generar una cadena de ARN mensajero complementaria a ese ADN. Después, esa secuencia de ARNm saldrá al citoplasma de la célula, donde se comportará como las vacunas de ARNm, para generar la proteína S del virus. En el caso de la vacuna de Oxford-AstraZeneca, este ADN se inserta en un adenovirus de mono, de forma que este adenovirus entra en la célula y acaba introduciendo ese ADN en el núcleo. El listado de vacunas que usan adenovirus es el siguiente:
- CanSino Biologics (Ad5)
- AstraZeneca (Adenovirus de chimpancé)
- Stabilitech BioPharma (Ad5 oral)
- ImmunityBio (Ad5 de 2ª generación)
- ReiThera (Adenovirus de gorila)
- Janssen (Ad26)
- Altimmune (Ad5 intranasal)
- Vaxart (Ad5 oral)
- Sputnik V (Ad26 y Ad5)
También usa el mismo sistema la vacuna rusa Sputnik V, como puedes ver en esta infografía disponible en su web.

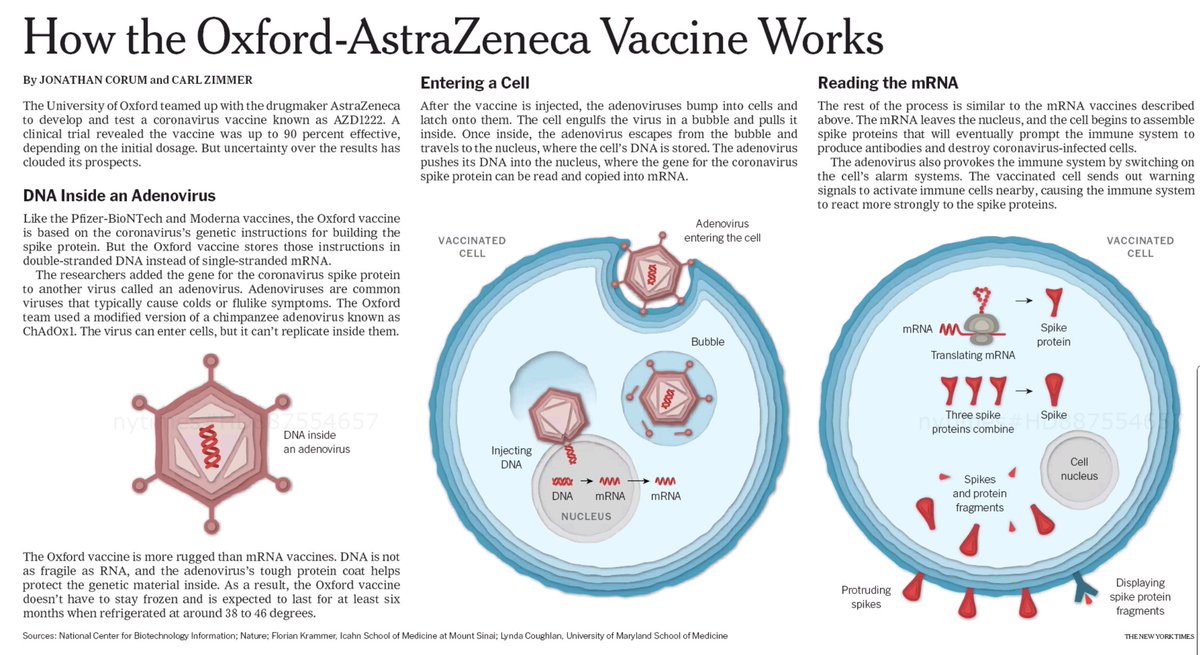
La vacuna JNJ-78436735 o Ad26.CoV2.S de la farmacéutica con sede en Bélgica Janssen (Johnson & Johnson), en colaboración con el Beth Israel Deaconess Medical Center, también es otro ejemplo de vacuna de ADN. Se agregó el ADN al adenovirus 26 modificado, que puede ingresar a las células pero no puede replicarse dentro de ellas ni causar enfermedades.

Fuente: The New York Times
En julio, se aprobó la primera vacuna de este tipo para uso general en humanos, una vacuna contra el ébola, también fabricada por Johnson & Johnson, y también está desarrollando otras para el VIH y el Zika. Las vacunas basadas en adenovirus para Covid-19 son más resistentes que las vacunas de ARNm de Pfizer y Moderna. El ADN no es tan frágil como el ARN, y la dura capa de proteína del adenovirus ayuda a proteger el material genético en su interior. Como resultado, la vacuna de Johnson & Johnson se puede refrigerar hasta por tres meses a una temperatura de 36 a 46 °F (2 a 8 °C). Después de que es inyectada, los adenovirus chocan contra las células y se adhieren a las proteínas de su superficie. La célula envuelve el virus en una vesícula y lo empuja hacia adentro por endocitosis. Una vez dentro, el adenovirus escapa de la vesícula y viaja al núcleo, de la célula. El adenovirus está diseñado para que no pueda hacer copias de sí mismo, pero la célula puede leer el gen de ADN de la proteína del pico del coronavirus y copiarlo en una molécula de ARN mensajero.
 Fuente: The New York Times
Fuente: The New York Times
Después, el ARNm sale del núcleo y los ribosomas de la célula leen su secuencia y comienzan a fabricar las proteínas S.

Algunas de las proteínas S producidas por la célula migran a su superficie y sobresalen sus puntas. Las células vacunadas también descomponen algunas de las proteínas en fragmentos, que presentan en su superficie. Estos picos y fragmentos que sobresalen pueden ser reconocidos por el sistema inmunológico. Cuando una célula a la que llegó el adenovirus muere, sus restos contienen proteínas y fragmentos de proteínas que luego pueden ser absorbidos por un tipo de célula inmunitaria llamada célula presentadora de antígenos.

Fuente: The New York Times
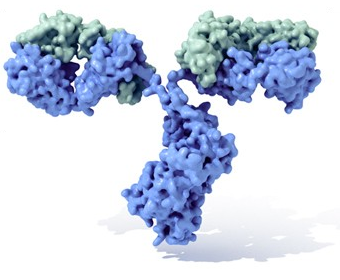
La célula presenta fragmentos de la proteína espiga en su superficie. Cuando otras células llamadas células T auxiliares detectan estos fragmentos, las células T auxiliares pueden dar la alarma y ayudar a organizar otras células inmunes para combatir la infección. Otras células inmunes, llamadas células B, pueden chocar con los picos de coronavirus en la superficie de las células vacunadas o con fragmentos de proteína de pico que flotan libremente. Algunas de las células B pueden fijarse en las proteínas de pico. Si estas células B son activadas por células T auxiliares, comenzarán a proliferar y a derramar anticuerpos que se dirigen a la proteína de pico.

Los anticuerpos pueden adherirse a los picos de coronavirus, marcar el virus para su destrucción y prevenir la infección al impedir que los picos se adhieran a otras células.

ANTICUERPOS
VIRUS
Las células presentadoras de antígenos también pueden activar otro tipo de célula inmunitaria llamada célula T asesina para buscar y destruir cualquier célula infectada por coronavirus que muestre los fragmentos de proteína en punta en sus superficies.

Con respecto a este novedoso tipo de vacunas, cabe recalcar que hasta la aparición de las vacunas para COVID-19, ninguna vacuna de adenovirus se había usado comercialmente con humanos y solo había una vacuna veterinaria para la rabia (ONRAB), aunque se llevan creando vectores adenovirales desde los años 80, en especial, con Adenovirus 5. Hacia 1999 se descartó también su uso en terapia génica cuando un adolescente falleció tras recibir una inyección de Ad5. También fracasó su uso para una vacuna contra el VIH (ver noticia). Más adelante, la empresa china CanSino, creó una vacuna para el ébola, que conseguía inducir anticuerpos al mes de su inoculación, aprobándose para su uso de emergencia en 2017 en China, convirtiéndose en la primera vacuna adenoviral aprobada para humanos, aunque con ciertas dudas pues los anticuerpos bajaban notablemente al medio año de la vacunación. Esta experiencia previa le permitió avanzar en su desarrollo para una vacuna contra COVID-19.
Janssen también desarrolló una vacuna experimental para el ébola, administrada en personas de la República Democrática del Congo y Ruanda, pero basada en el Adenovirus 26. Un problema de estos adenovirus es que la población pueda tener inmunidad preexistente contra ellos, por lo que las vacunas basadas en ellas podrían no funcionar bien.
Oxford sin embargo se decantó por usar adenovirus de chimpancés, para desarrollar una vacuna contra la malaria, creando su propio vector viral (ChAdOx1), basado en virus de las heces de chimpancé. Desarrollaron varias vacunas experimentales, entre ellas, una contra el MERS que no tuvo éxito, pero que le permitió avanzar en su vacuna contra el COVID-19.
Al parecer, un problema que suelen presentar las vacunas de vector adenovirus es que su respuesta de anticuerpos no es tan fuerte como la de otras vacunas más tradicionales.
VACUNAS DE ANTÍGENO
En este tipo de vacunas en desarrollo (por ejemplo, la vacuna NVX-CoV2373 de Novavax), lo que se inocula es directamente "copias" de la proteína S del virus, para estimular la producción de anticuerpos neutralizantes. Para ello, se crea un ADN a partir del fragmento de ARN del virus que codifica la proteína S, después se une a otro fragmento de ADN más grande, para introducir esos genes después en células en el laboratorio. Estas células leen el ADN, lo convierten en ARNm y luego fabrican las proteínas (igual que sucede con las vacunas de vectores virales, pero en células externas al organismo). Después, se recolectan las proteínas y purifican para añadirlas a la vacuna, donde se unen a lo que se llama un vehículo de liberación (partículas sintéticas o nanopartículas, del tamaño aproximado de un virus). Esta técnica ya se ha probado en vacunas modernas (desde 1986) con buenos resultados (gripe o hepatitis B), pero su desarrollo es más lento que las de ARNm, que por ello se aprobaron antes. Necesitan además un adyuvante, que es un ingrediente extra para potenciar la respuesta inmunológica frente al antígeno (proteína S en este caso). En estudios preliminares, esta vacuna mostró inmunidad esterilizante (protegiendo vías respiratorias), lo cual prevendría de la infección, y no solo de la enfermedad grave, y, por tanto, frenaría las cadenas de contagio (ver artículo).
En el caso concreto de la vacuna de Novavax, los primeros ensayos mostraron niveles de anticuerpos sorprendentes, que excedieron los niveles de anticuerpos en suero de pacientes convalecientes (ver estudio). Para crear su vacuna, los investigadores de Novavax comenzaron con un gen de pico modificado. Insertaron el gen en un virus diferente, llamado baculovirus , y le permitieron infectar células de insectos. Las células infectadas produjeron las proteínas espiga, de forma similar a lo que harían las vacunas de vectores virales de ADN, pero en lugar de hacerlo nuestras células, las fabrican células de insectos.

Fuente: The New York Times
Después de este proceso, se recolectan las proteínas de las células de los insectos y se ensamblan como nanopartículas. Si bien las nanopartículas imitan la estructura molecular del coronavirus, no pueden replicarse ni causar COVID-19.

Fuente: The New York Times
Esta vacuna se inyecta en los músculos del brazo. Cada inyección incluye muchas nanopartículas, junto con un compuesto extraído del árbol de la corteza de jabón, denominado adyuvante. La misión de este compuesto es atraer a las células inmunitarias y hacer que respondan con más fuerza a las nanopartículas.

Fuente: The New York Times
Más adelante, las células inmunes llamadas células presentadoras de antígenos encuentran las nanopartículas de la vacuna y las absorben. Estas células presentadoras de antígeno desgarran las proteínas de la nanopartícula, y muestra algunos de sus fragmentos en su superficie. De este modo, los linfocitos T colaboradores pueden detectar los fragmentos, y si un fragmento encaja en una de sus proteínas de superficie, la célula T se activa, induciendo así la respuesta inmunológica.

Fuente: The New York Times
Más tarde, otro tipo de célula inmunitaria, los linfocitos B, también puede encontrarse con las nanopartículas de la vacuna. Las células B tienen proteínas de superficie en una gran variedad de formas, y algunas podrían tener la forma correcta para adherirse a una proteína S. Si una célula B se adhiere, puede empujar la partícula de la vacuna hacia adentro y presentar fragmentos de proteína en forma de pico en su superficie. Si una célula T colaboradora activada contra la proteína S se adhiere a uno de estos fragmentos, activa la célula B. Entonces la célula B prolifera y derrama anticuerpos que tienen la misma forma que sus proteínas de superficie.

Fuente: The New York Times
Si las personas vacunadas se exponen más tarde al coronavirus, sus anticuerpos pueden bloquear las proteínas S del virus, por lo que no puede ingresar a las células y la infección está bloqueada.

Fuente: The New York Times
La vacuna Novavax también puede activar otro tipo de protección al destruir las células infectadas. Cuando un coronavirus invade, las células infectadas colocan fragmentos de su proteína en punta en su superficie. Las células presentadoras de antígenos pueden activar un tipo de célula inmunitaria llamada célula T asesina. Puede reconocer células infectadas y destruirlas antes de que tengan la oportunidad de producir nuevos virus.

Fuente: The New York Times
VACUNAS CON VIRUS ATENUADOS
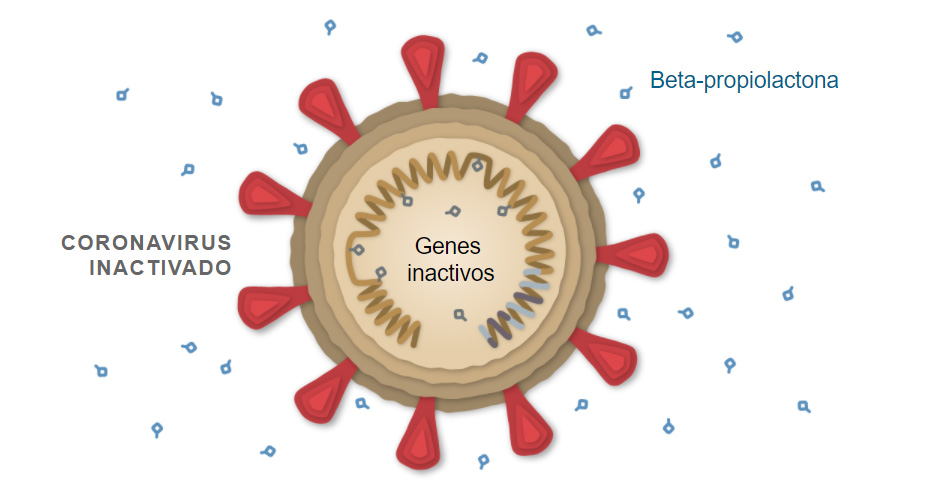
Después, los investigadores extrajeron los virus inactivados y los mezclaron con una pequeña cantidad de un compuesto adyuvante a base de aluminio, compuesto este usado para estimular el sistema inmunológico de cara a la respuesta a una vacuna. Los virus inactivados se han utilizado durante más de un siglo, de forma que otras vacunas como la de la polio (años 50), la rabia o la hepatitis A. Debido a que los virus inoculados están inactivos, pueden inyectarse en el brazo sin causar la enfermedad. Una vez dentro del cuerpo, algunos de estas unidades de virus inactivados son digeridos por las células presentadoras de antígenos.

Fuente: New York Times
La célula presentadora de antígeno desgarra el coronavirus y muestra algunos de sus fragmentos en su superficie, De forma que las células T colaboradora pueden detectar el fragmento de la proteína S, y la célula T se activa y puede ayudar a reclutar otras células inmunes para responder a la vacuna. Las llamadas células B, también pueden encontrarse con el coronavirus inactivado. Las células B tienen proteínas de superficie en una gran variedad de formas, y algunas podrían tener la forma correcta para adherirse al coronavirus. Cuando una célula B se bloquea, puede arrastrar parte o todo el virus al interior y presentar fragmentos de coronavirus en su superficie. Una célula T colaboradora activada contra el coronavirus puede adherirse al mismo fragmento. Cuando eso sucede, la célula B también se activa. Prolifera y derrama anticuerpos que tienen la misma forma que las proteínas de su superficie.

Fuente: New York Times
Una vez vacunado con CoronaVac, el sistema inmunológico puede responder a una infección de coronavirus vivos. Las células B producen anticuerpos que se adhieren a los virus activos invasores. Los anticuerpos que se dirigen a la proteína de pico pueden evitar que el virus ingrese a las células. Otros tipos de anticuerpos pueden bloquear el virus por otros medios.
Fuente: New York Times
Si bien CoronaVac puede ofrecer cierta protección contra Covid-19, nadie puede decir aún cuánto dura esa protección. Es posible que el nivel de anticuerpos disminuya en el transcurso de meses. Pero el sistema inmunológico también contiene células especiales llamadas células B de memoria que pueden retener información sobre el coronavirus durante años o incluso décadas.
Otras vacunas de virus inactivados son la de Sinopharm (China) y Covaxin (India), que presentó eficacia media del 78%, 100% frente a la enfermedad grave y 70% frente a infección asintomática en el ensayo clínico fase III, siendo eficaz también frente a las variantes, incluyendo las de doble mutación (ver artículo).
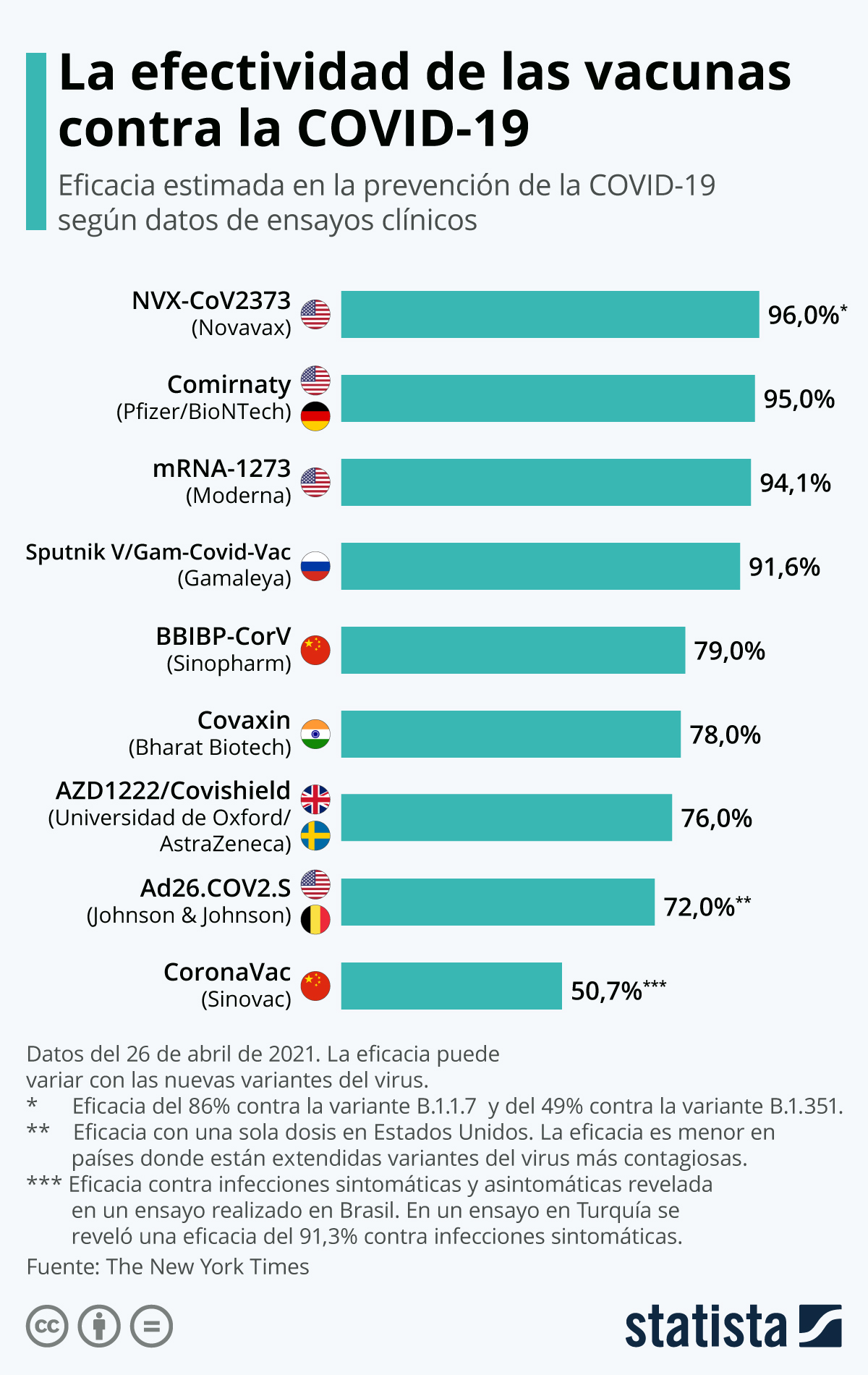
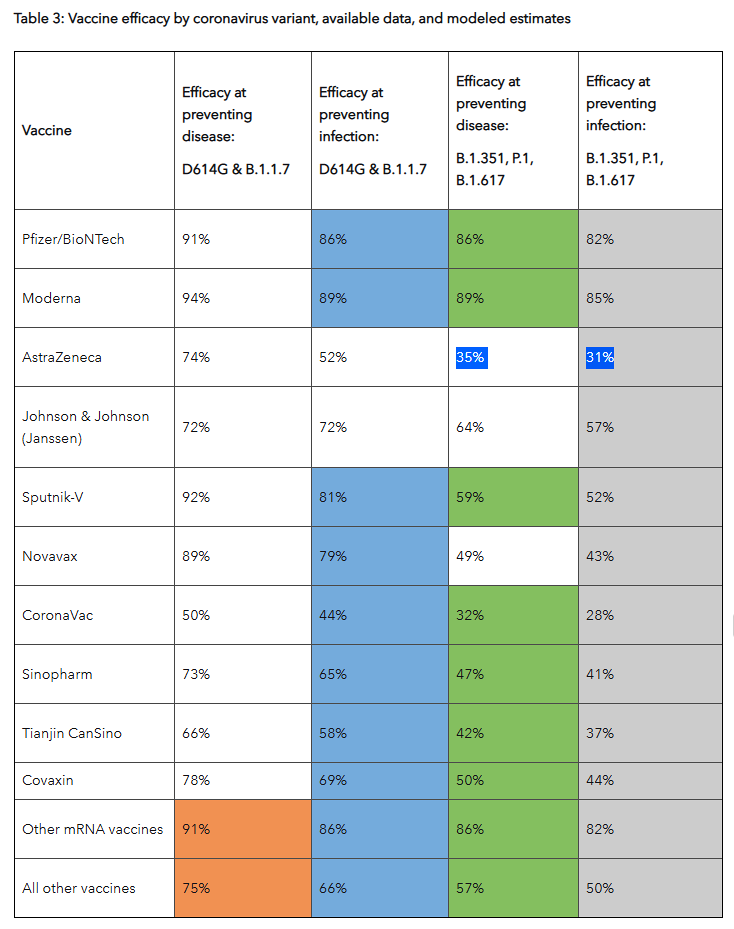
EFECTIVIDAD CONTRA VARIANTES
Fuente: HealthData
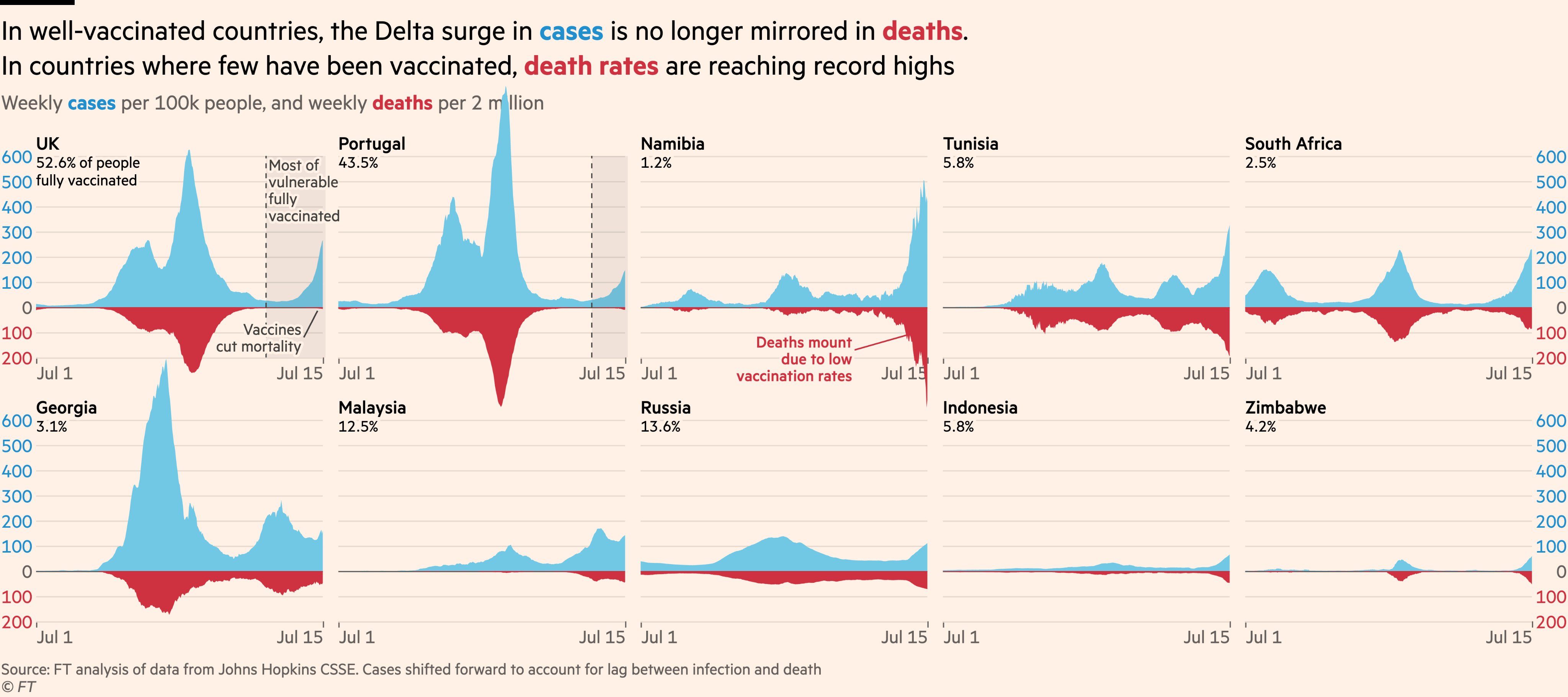
Sobre la efectividad de las vacunas en la vida real en relación a la mortalidad, es interesante ver este gráfico elaborado por John Burn-Murdoch en julio de 2021. En el se puede ver claramente que en países con alta tasa de vacunación (más del 40%), las muertes (en rojo) eran muy pocas en relación a la subida de casos (en azul). En países con poca tasa de vacunación, las muertes eran significativamente más altas en proporción con el número de casos. En el Reino Unido, las vacunas habían reducido la tasa de letalidad aproximadamente 12 veces, aproximadamente de un 2% a 0,16%. En Namibia, Túnez, Malasia e Indonesia, las tasas de mortalidad nunca habían sido tan altas. Sin embargo, la relajación de medidas prematura en países con alta tasa de vacunación, estaba provocando una subida de casos y por tanto, un aumento también de las muertes, aunque en menor medida.


















 Factores de riesgo
Factores de riesgo Técnicas de detección
Técnicas de detección Tratamientos
Tratamientos Vacunas
Vacunas Carga viral
Carga viral Mutaciones
Mutaciones Letalidad y mortalidad
Letalidad y mortalidad Prevención: mascarillas
Prevención: mascarillas Prevención: Ventilación y filtración (HEPA)
Prevención: Ventilación y filtración (HEPA) Otras medidas de prevención
Otras medidas de prevención Impacto de la pandemia
Impacto de la pandemia Fin de la pandemia
Fin de la pandemia Prevención en centros educativos
Prevención en centros educativos Enlaces de interés
Enlaces de interés





