Última actualización: 26 de abril de 2021
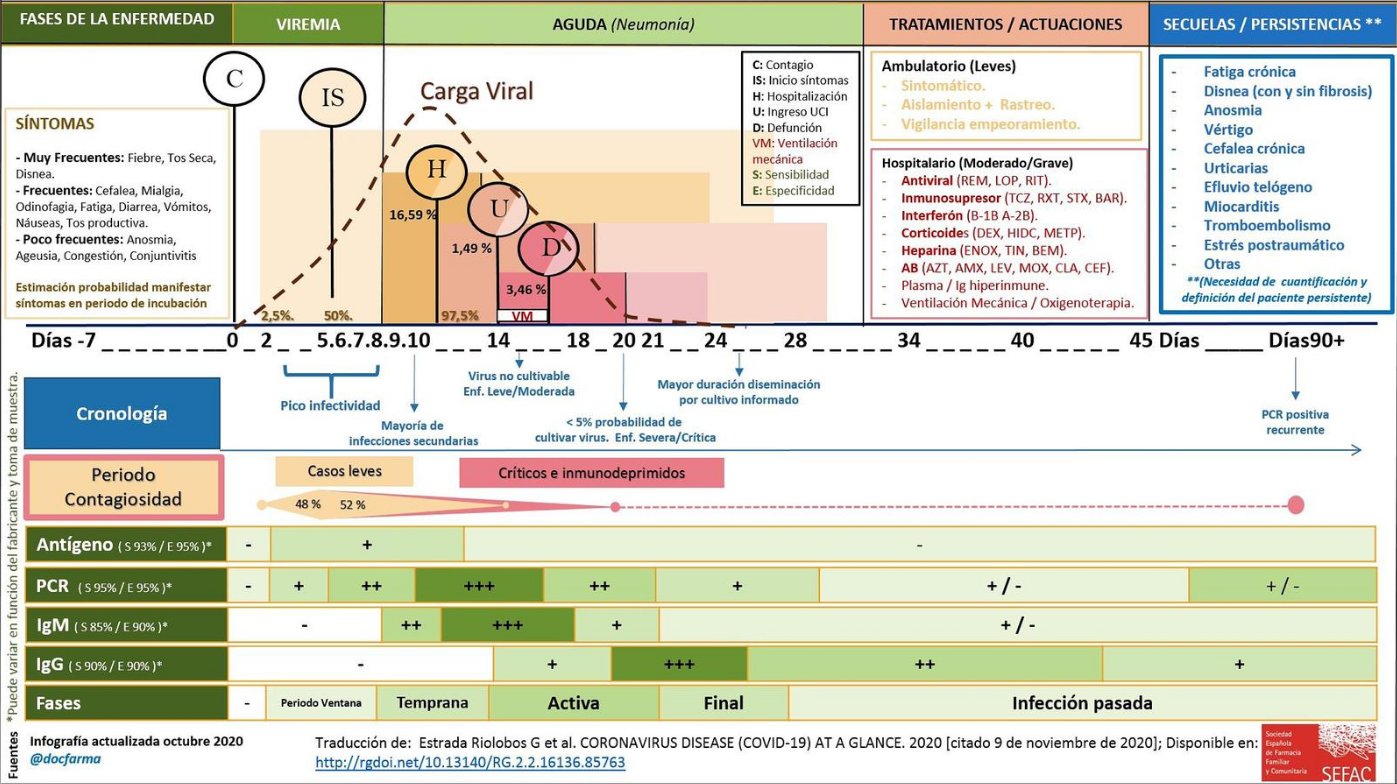
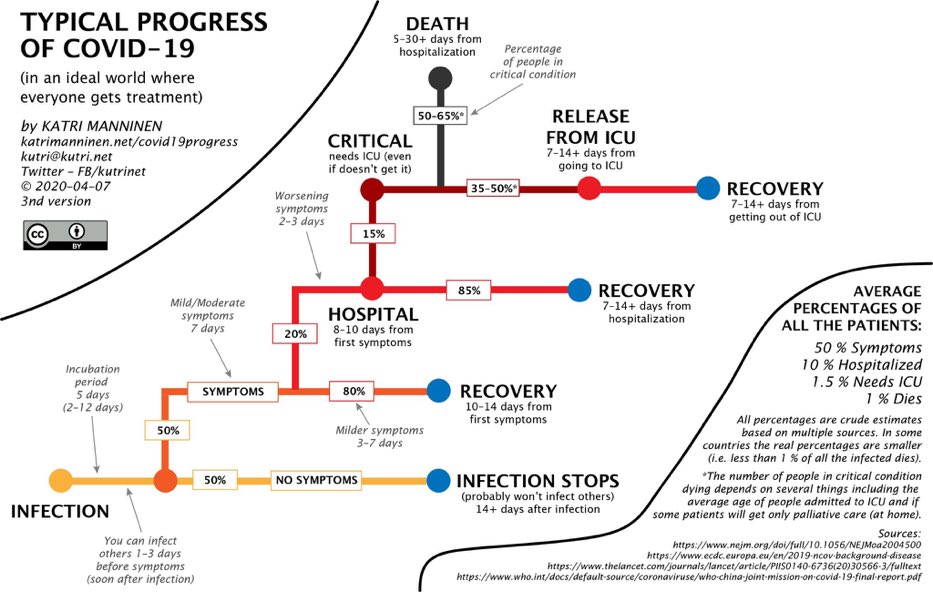
Según parece, la COVID-19 puede tener hasta tres fases de evolución, que podemos ver en la siguiente infografía:
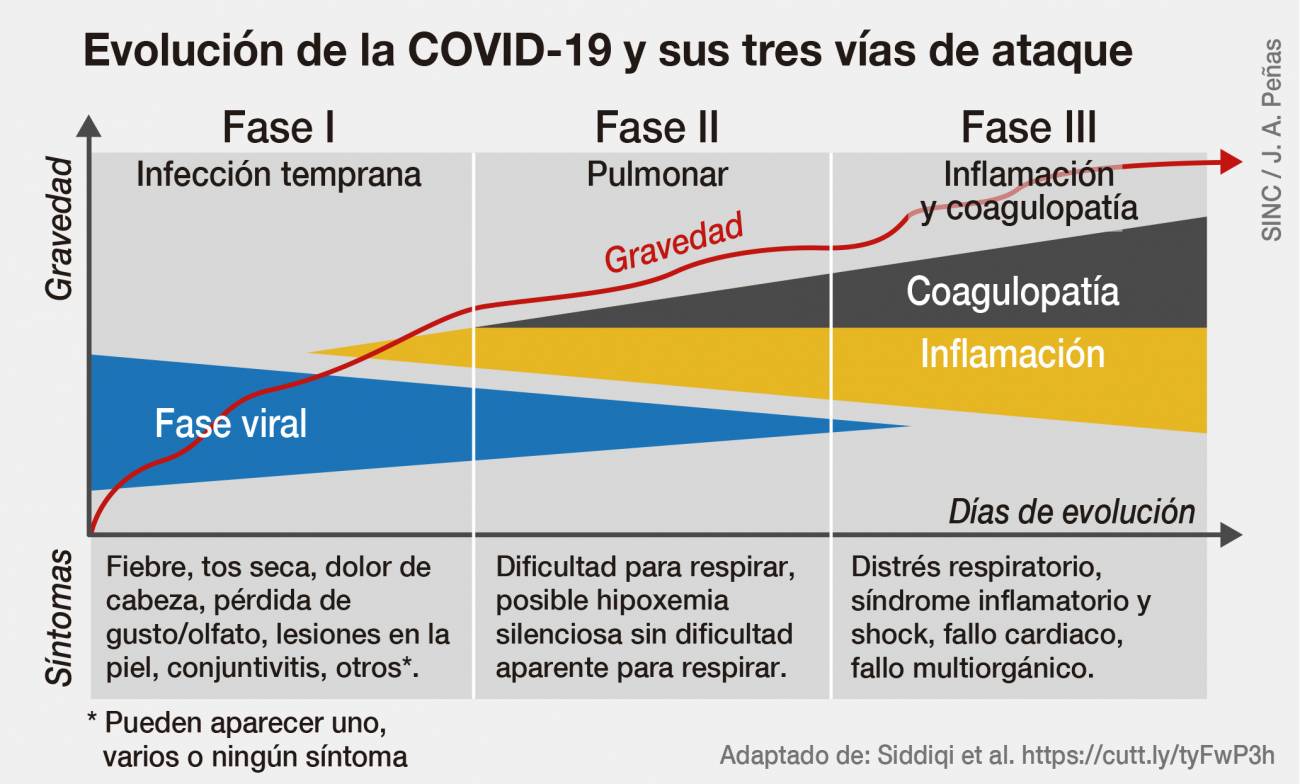
Fuente: agenciasinc
Desde que se produce el contagio hasta que se empiezan a desarrollar síntomas, transcurre el denominado periodo de incubación, en el que, a diferencia de otras infecciones, el paciente puede contagiar a otras personas de forma silenciosa. Estudios cifraron en los primeros meses de pandemia el periodo de incubación medio en 5 días, si bien podría dilatarse hasta los 11 días, o en casos muy excepcionales, más de 14 días (ver artículo). Es por esto por lo que desde las autoridades españolas, se recomendaba una cuarentena de 14 días en caso de manifestar síntomas. En otros países, como Reino Unido, las cuarentenas fueron inicialmente de tan solo 7 días, teniendo que ser ampliadas a 10 días con posterioridad a finales de julio por ser insuficientes (ver noticia). Sin embargo, en agosto, científicos chinos apuntaban a que sería mayor, dando estimación media de 7,76 días, más larga que las estimaciones anteriores de 4 a 5 días, siendo significativo que hasta el 10% de los pacientes estudiados mostraron un periodo de incubación medio levemente superior a los 14 días recomendados de cuarentena (ver noticia). Otro estudio encontró casos en los que duró hasta 17 días, y no solo eso, sino que una persona podría empezar a contagiar tan solo 2 días después de infectarse, por lo que una persona puede contagiar durante el periodo de incubación (ver estudio).
En diciembre, un estudio sugería que la gravedad de la enfermedad podría depender de la vía de contagio. Se hizo un experimento con hámsteres sirios, susceptibles a la infección por SARS-CoV-2, a través de exposición intranasal, aerosol y fómites. Las diferentes vías de exposición se presentaron con distintas manifestaciones de la enfermedad. La inoculación intranasal y en aerosol causó una patología respiratoria más grave, mayores cargas de virus y una mayor pérdida de peso. La exposición a los fómites condujo a una manifestación de la enfermedad más leve. La transmisión aérea era más eficiente que la transmisión vía fómite y dependía de la dirección del flujo de aire (ver estudio).
La fase I corresponde a una fase temprana o fase viral, iniciada nada más producirse el contagio. Estudios científicos han cifrado hasta en torno a un 80% los casos de personas que contraen el virus y solo atraviesan esta fase, de forma que o bien no desarrollan síntomas y pasan el virus de manera asintomática, o bien desarrollan algunos síntomas considerados como leves, muy probablemente porque su sistema inmunitario ofrece una adecuada respuesta al virus y a la carga viral contraída. Conforme han pasado los meses, se han ido conociendo más síntomas asociados a esta fase, entre los cuales destacan:
- Fiebre, tos, disnea: desde febrero y marzo de 2020, se empieza a informar por parte de los organismos oficiales que estos tres son los síntomas más comunes. Así constaba en casi todas las infografías informativas de organismos oficiales. Según el caso, también se podía presentar dolor de garganta o de cabeza.
- Anosmia o hiposmia (pérdida de olfato total o parcial) y ageusia (pérdida del gusto): estos síntomas pueden durar bastante tiempo, incluso el gusto y el olfato pueden ir recuperándose poco a poco pero no por completo. Estudios sugieren que la anosmia y ageusia están presentes en más del 80% de casos (ver noticia), por lo que se consideran síntomas claramente patognomónicos. Un estudio concluyó que la pérdida de olfato se diferencia de la que sucede en caso de resfriados comunes porque la persona la manifiesta pudiendo respirar libremente, sin tener taponada la nariz (ver artículo). Otro estudio elaborado en Reino Unido concluyó que la pérdida de olfato es un síntoma altamente específico de la COVID-19, que puede darse sin presentar tos ni fiebre y que debería ser tomado en consideración siempre para proceder al testeo, aislamiento y tratamiento en su caso de la enfermedad (ver estudio). Otro estudio sobre la anosmia publicado en enero de 2021 concluyó que es más prevalente en las formas leves de COVID-19 (85'9%) que en las formas moderadas o críticas, soliendo desaparecer en el 95% de los pacientes en un plazo de hasta 6 meses (ver estudio).
- Diarrea, vómitos, fatiga, congestión nasal, náuseas, afonía, cefaleas, dolor muscular, escalofríos, dolor torácico, mucosidad...: conforme van llegando casos graves a los hospitales, se empieza a ver que eran muy comunes síntomas como fuertes diarreas, una importante fatiga que imposibilitaba incluso los desplazamientos, así como la pérdida de olfato (anosmia) y la pérdida del gusto (ageusia). También, tras los primeros meses, se consideraron importantes los síntomas gastrointestinales, pues hasta el 60% de los pacientes los desarrollaban y no se relacionaban con COVID-19, no siendo testados y favoreciendo así que pudieran propagar el virus (ver noticia). El abanico de síntomas es muy diverso, y no solo son comunes fiebre, tos o disnea como se pensaba en un principio. También se cree que incluso un fuerte hipo podría ser síntoma del virus (ver noticia).
- Exantemas o rashes cutáneos, acroisquemia digital en los pies y conjuntivitis: también se han descrito estos síntomas en pacientes de COVID-19, destacando también su presencia en niños (ver noticia). Un estudio llevado a cabo por investigadores del New York Presbyterian Hospital y el Weill Cornell Medical College sugiere que las afecciones cutáneas en casos severos pueden ser un indicio de un estado trombótico subyacente, por lo que es preciso el tratamiento con anticoagulantes en caso de detectar esta sintomatología (ver estudio). En el caso de niños y adolescentes, se empezó a detectar en Italia niños con acroisquemia digital en los pies y se relacionó con la COVID-19 (ver artículo), aunque estudios posteriores en España venían a decir que era pura coincidencia y no estaba probada la relación (ver estudio en España), y también en Bélgica, porque no se detectaba el virus en PCR o muestras de piel de la mayoría de pacientes examinados (ver estudio en Bélgica). No obstante, en junio se publicó otro estudio en el que se indicaba que, en un cohorte de 7 niños de 11 a 17 años con este tipo de lesiones, con PCR negativa, se practicaron test de anticuerpos en biopsias extraídas de los tejidos dañados, siendo positivas en el 100% de los casos, y, además, una de las biopsias se examinó en el microscopio, encontrándose partículas de tipo vírico, por lo que la conclusión obtenida es que este tipo de lesiones sí están vinculadas al SARS-CoV-2 (ver estudio).

Acroisquemia digital. Fuente: podoactiva.com
- Depresión o ansiedad: algunos estudios indican que cuadros depresivos o de ansiedad también se han dado como síntomas en pacientes de COVID-19 (ver noticia).
- Lengua COVID: en enero de 2021, se dio a conocer otro posible síntoma, en base a un estudio realizado en abril de 2020 en el Hospital de Campaña de IFEMA en Madrid (ver estudio). En dicho estudio, se encontraron unas alteraciones en la lengua tales como un agrandamiento de la misma, en la que se pueden ver las marcas de los dientes, pudiendo estar incluso depapilada, y con manchas rosadas. Se estudió a 666 pacientes ingresados entre el 10 y el 25 de abril de 2020, y más del 25% de los pacientes presentaba además otras alteraciones (papilitis lingual transitoria, úlceras bucales, sensación de ardor).

Fuente: Diario de Cádiz
- Hipoxia silenciosa/hipoxemia: la hipoxemia es un nivel de oxígeno en sangre inferior al normal. Han llamado particularmente la atención casos en los que existe falta de oxígeno en sangre, pero el paciente no es consciente de ello ni tampoco muestra disnea, lo cual es muy peligroso porque los órganos no se están oxigenando bien (ver noticia). Para ver la saturación de oxígeno en sangre, es decir, el nivel de oxígeno en la misma, se puede utilizar unos pequeños aparatos, denominados oxímetro o pulsioxímetro (el pulsioxímetro también detecta las pulsaciones por minuto), que se colocan en un dedo. Un valor normal de saturación en este tipo de aparatos oscila entre 95 y 100. Los valores inferiores a 90 /92 se consideran anómalos.

Fuente: oximetro.com.mx
La sintomatología es tremendamente variada, y aunque hay síntomas más comunes, también se han dado casos con síntomas que son mucho menos frecuentes. Por ejemplo, un varón fue diagnosticado de COVID-19 a partir de una orquitis, inflamación de los testículos (ver noticia). En la siguiente infografía de Mónica Lalanda puedes ver resumidos los más frecuentes.
En Reino Unido se llevó a cabo un estudio sobre los síntomas que desarrollaron 651 menores ingresados en 138 hospitales (ver estudio). Los síntomas más frecuentes fueron fiebre (70%), tos (39%), náuseas (32%) y disnea (30%), aunque como se puede ver en la siguiente imagen, la sintomatología incluye muchos síntomas diversos, muy comunes a otras dolencias, como fatiga, dolor abdominal, diarrea, erupciones cutáneas, rinorrea, dolor de cabeza, dolor de garganta, sibilancias, dolor muscular, confusión, esputo, conjuntivitis, linfopenia, dolor de articulaciones, convulsiones, sangrados o dolor de oído. Este estudio también mostraba que en este rango de edad una enfermedad severa era poco frecuente, y la muerte extremadamente poco frecuente.,

Fuente: thebmj
En agosto, investigadores de la Universidad del Sur de California publicaron el probable orden de aparición de síntomas comunes de la enfermedad, hallando que el primer síntoma suele ser la fiebre, seguida de tos y dolor muscular, para dar paso más adelante a nauseas, vómitos y diarrea (ver noticia). No obstante, cada caso es distinto, pudiendo mostrar algunos de estos síntomas y otros no, y desarrollar otros síntomas de los anteriormente mencionados.
La Universidad Complutense publicó antes del otoño de 2020 esta interesante infografía para tratar de diferenciar los síntomas más comunes de gripe, COVID-19, resfriado común y alergia.
Sin embargo, como se ha comentado, no todos los contagiados desarrollan síntomas, cobrando especial importancia aquí los pacientes asintomáticos, que se convertirían en contagiadores silenciosos que favorecen la propagación del virus (al igual que los presintomáticos, que son aquellos contagiados que pueden contagiar antes de desarrollar los síntomas). Algunos estudios cifran en un 30% el porcentaje de pacientes que contraen el virus pero no desarrollan síntomas (un 55% síntomas leves, un 10% síntomas severos, y un 5% síntomas críticos). Otros estudios cifran en hasta un 45% el porcentaje de asintomáticos (ver noticia), y en el caso de la ciudad italiana de Vo', un estudio arrojaba un 42,5% de infecciones asintomáticas (ver estudio). Otros estudios sobre infecciones en el hogar tasaba en un 18% el porcentaje de casos asintomáticos (ver artículo del CDC). También es interesante el caso del crucero Diamond Princess (ver noticia), en el que sobre un centenar de pacientes, un 78% inicialmente o no presentaban síntomas o tenían síntomas leves. Con respecto a los asintomáticos también se han hecho estudios, detectándose que sus anticuerpos duran menos, que son contagiosos durante más tiempo, o que presentan cargas virales similares a los casos más graves (ver estudio). Pero lo más preocupante es la existencia de estudios que demuestran que, pese a pasar la enfermedad de forma asintomática, muchos acaban presentando anomalías en los pulmones al realizárseles pruebas diagnósticas como por ejemplo, una Tomografía Axial Computerizada (TAC), incluso en una proporción de casi un 60% (ver estudio) (ver estudio).

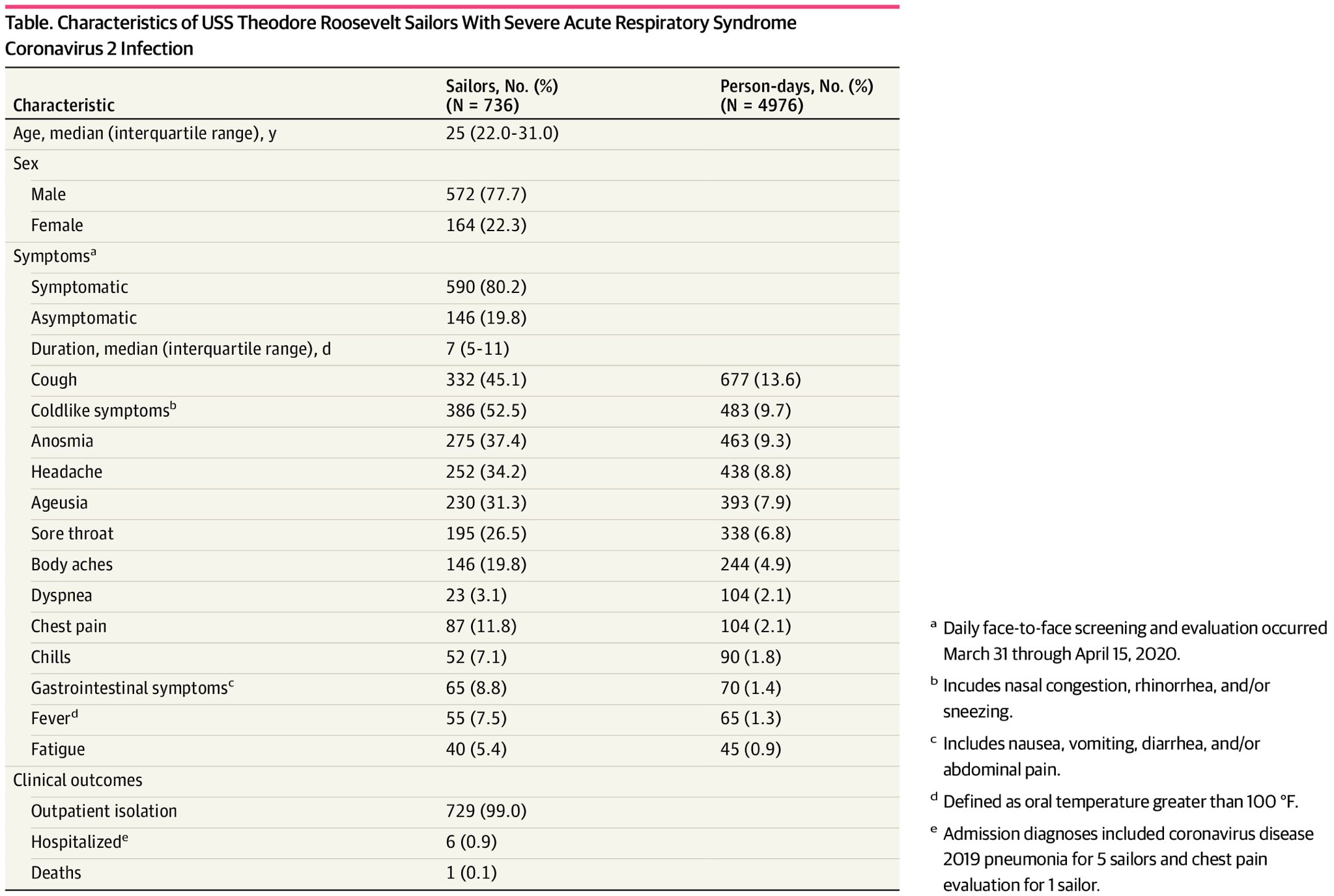
Un estudio de un brote en el portaaviones norteamericano Theodore Roosevelt arrojó datos interesantes, aunque no extrapolables al total de la población, ya que la edad media era de 25 años. Cerca del 20% de contagiados fueron asintomáticos, y entre los sintomáticos, los síntomas más frecuentes fueron tos, síntomas de resfriado (congestión, rinorrea, ...), anosmia, dolor de cabeza, ageusia y dolor de garganta (ver estudio).
En la era de la tecnología, como no podía ser de otra manera, hay incluso científicos que están diseñando un wearable, parecido a una tirita, que se pone en la garganta, con el fin de detectar síntomas de la enfermedad y alertar en caso necesario (ver artículo).
/https://public-media.si-cdn.com/filer/0d/a7/0da7593d-44a7-4779-90ff-a020c57da882/john_rogers_covid-19_wearable.jpg)
Fuente: smithsonianmag.com
Si el organismo no ha podido emitir una respuesta inmune suficiente durante la fase I, comenzaría la fase II o fase pulmonar, en la que la gravedad empieza a ser moderada. En estos casos, es acusada la tos, la fiebre y la dificultad respiratoria, ya que se origina una inflamación pulmonar tanto por la presencia del virus como por la respuesta de nuestro organismo. La mayoría de pacientes que requieren hospitalización en esta fase acaban superando la infección (algunas estimaciones hablan del 15%).
Los cuadros más graves, con ingreso hospitalario, suelen incluir neumonías bilaterales. Especialmente los casos graves, se desarrollan neumonías bilaterales galopantes con un patrón radiológico característico: afectación bilateral (en ambos pulmones), localización externa (no cerca del hilio sino por los bordes), y en forma de 'vidrio esmerilado', que representa zona infección.

Hilio pulmonar. Fuente: Mi revista médica
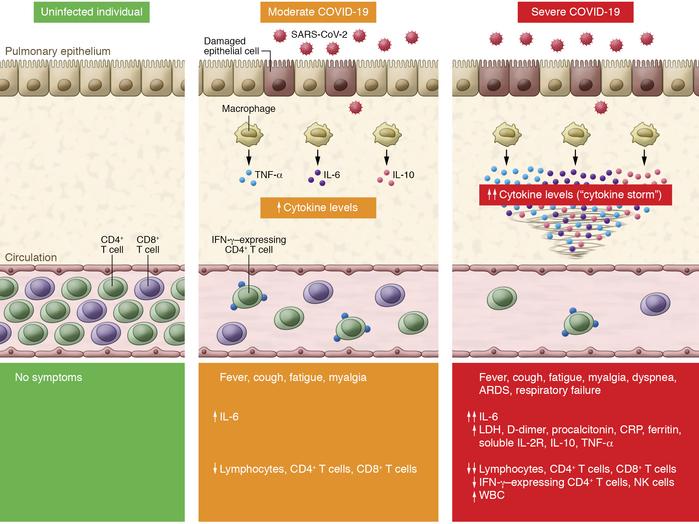
En los casos graves, las neumonías llegaban a ocupar por completo los pulmones, produciendo una gran disminución de la saturación de oxígeno. Las gafas nasales mascarillas de oxígeno pueden no ser suficientes, por lo que, en casos graves, hay que proceder a una intubación en UCI. Estas se producen porque el sistema inmune genera una tormenta de citoquinas; en una neumonía normal, el sistema inmunitario genera una respuesta inflamatoria para detenerla, mientras que en una neumonía con COVID 19, la reacción del sistema inmunitario es desproporcionada e incontrolada, dañando no solo al virus, sino a las células del propio organismo. Algunos estudios sugieren que determinados pacientes no pueden sentir la falta de oxígeno generada (hipoxia) debido a que el propio virus también ataca al sistema nervioso central, alterando así la percepción del cerebro. Algunas de estas neumonías se pueden sobreinfectar con bacterias. El análisis de sangre en esta fase revela que existe linfopenia (un recuento anormalmente bajo de linfocitos en la sangre), junto con el aumento de transaminasas (enzimas que se se encuentran en células de órganos vitales como hígado, corazón, músculos o riñones).

En el siguiente vídeo puedes ver cómo ataca el virus provocando las temidas neumonías.
La siguiente imagen, publicada en el New England Journal of Medicine, ilustra perfectamente la infección del virus en los pulmones. Proviene del laboratorio de la neumóloga pediátrica Camille Ehre, de la Universidad de Carolina del Norte. Su equipo capturó esta instantánea de los virus del SARS-CoV-2 que salen de las células pulmonares en una placa de laboratorio. Primero cultivaron células del revestimiento de las vías respiratorias humanas y luego las inocularon con el virus. Noventa y seis horas después, esto es lo que vieron en escala de grises. Los colores vivos fueron agregados más tarde por el estudiante de medicina de la UNC, Cameron Morrison. La imagen ilustra la asombrosa cantidad de partículas virales que se pueden producir y liberar a partir de células humanas infectadas. Ehre señala que en una placa de laboratorio que contiene alrededor de un millón de células humanas, han sido testigos de cómo el virus explotó de alrededor de 1,000 partículas a alrededor de 10 millones en solo un par de días. El dramático aumento de partículas virales ayuda a explicar cómo el COVID-19 se propaga tan fácilmente de los pulmones a otras partes del cuerpo y, con demasiada frecuencia, a otras personas, especialmente en lugares cerrados y abarrotados donde la gente no puede quedarse. su distancia.
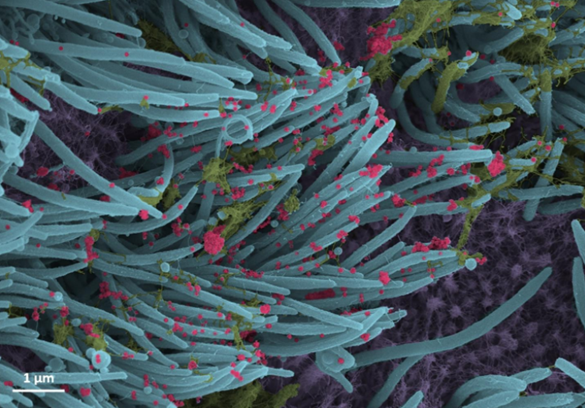
Radiológicamente, el aspecto de unos pulmones afectados por un cuadro grave de COVID-19 tienen bastante peor aspecto que los pulmones de un fumador que consume muchos cigarrillos al día, como puedes ver en la siguiente imagen.
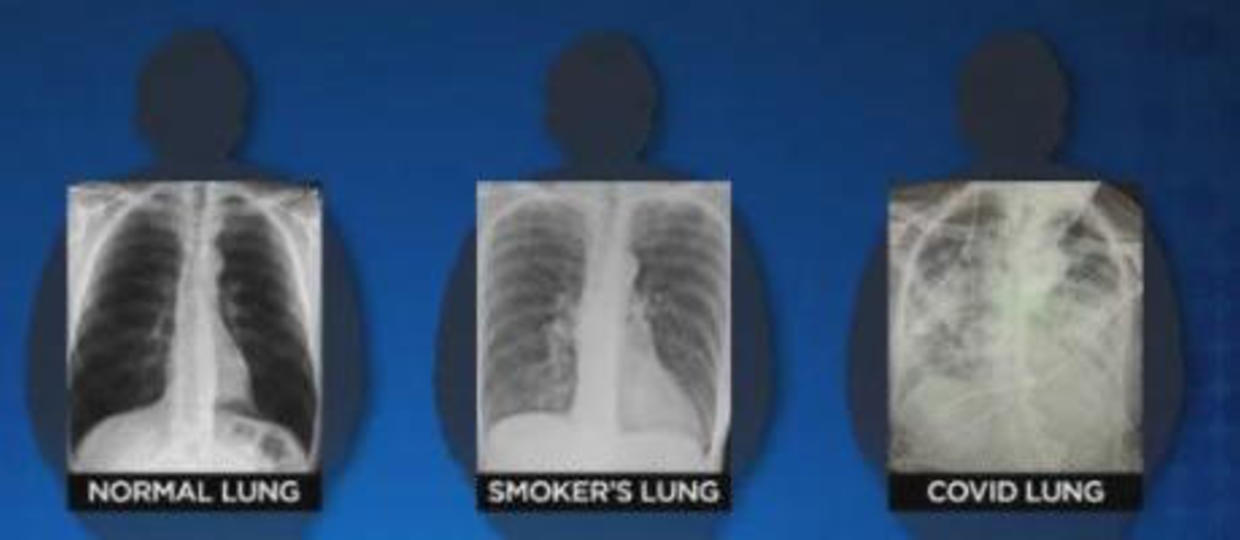
Radiografías de un pulmón normal, el pulmón de un fumador y el pulmón de un paciente con COVID. Fuente: DR. BRITTANY BANKHEAD-KENDALL VÍA CBS DALLAS
Para ayudar al diagnóstico de la COVID-19 con una simple radiografía, se han llegado a crear aplicaciones de inteligencia artificial, que puede determinar con qué probabilidad la imagen diagnóstica corresponde al coronavirus, a una neumonía por otras causas, o incluso si corresponde a un paciente sano. Un ejemplo se puede encontrar en www.coronavirusxray.com, aplicación web desarrollada por estudiantes del último curso de Ingeniería de la Universidad Europea de Madrid.

Si la infección no logra frenarse en la fase II, se pasa a la fase III, que es una fase hiperinflamatoria en la que se presenta una inflamación generalizada en el organismo debido a la tormenta de citoquinas, así como posibles coagulopatías, quedando afectados pulmones y posiblemente otros órganos como corazón, sistema nervioso y riñones principalmente. Estos pacientes requieren cuidados críticos. En esta fase la letalidad podría rondar el 50%. Varios estudios han demostrado que las citoquinas inflamatorias y biomarcadores como la ferritina y el dímero D están significativamente elevados en aquellos pacientes con enfermedad más grave. Un valor alto de ferritina (que es una proteína que almacena en las células el hierro necesario para producir glóbulos rojos) se asocia con la presencia de una tormenta de citoquinas según estudios (ver artículo), y un valor alto de dímero D sugiere que hay una coagulopatía o problema de coagulación de a sangre. También hay otros marcadores elevados en esta fase (interleucinas, proteína inflamatoria de macrófagos 1-α, factor de necrosis tumoral α, la proteína C reactiva). Además, investigadores del Centro de Hígado de Yale (Estados Unidos) han encontrado que los pacientes con COVID-19 con pronóstico grave presentaban pruebas hepáticas anormales en una alta proporción, incluyendo niveles más altos de enzimas hepáticas, (proteínas liberadas cuando el hígado está dañado). Así, dependiendo de la prueba, oscilaban entre el 40 y el 80% los pacientes con niveles alto de aspartato aminotransferasa (AST) y alanina transaminasa (ALT), que indican la inflamación de las células hepáticas, un aumento en la bilirrubina, que indica disfunción hepática, y un aumento en los niveles de fosfatasa alcalina (ALP), que puede indicar inflamación de los conductos biliares (ver noticia).
Aunque la neumonía bilateral es la complicación más característica, y, por eso, se pensaba que el virus era principalmente respiratorio, se descubrieron más tarde en muchos pacientes daños cardíacos, hepáticos y renales, de forma que el virus puede provocar daños cardíacos como arritmias de distinta consideración (algunas requieren incluso una intervención quirúrgica posterior para subsanarlas). Un estudio que analizó situaciones de paro cardiaco en pacientes hospitalizados en UCIs con COVID-19, arrojó como conclusión que se tratan de casos con muy mal pronóstico general. De los 5019 pacientes estudiados, 701 tuvieron paro cardiaco, lo que supone casi un 14%, siendo en el 65% de los casos varones, con una media de edad de 63 años (ver estudio).

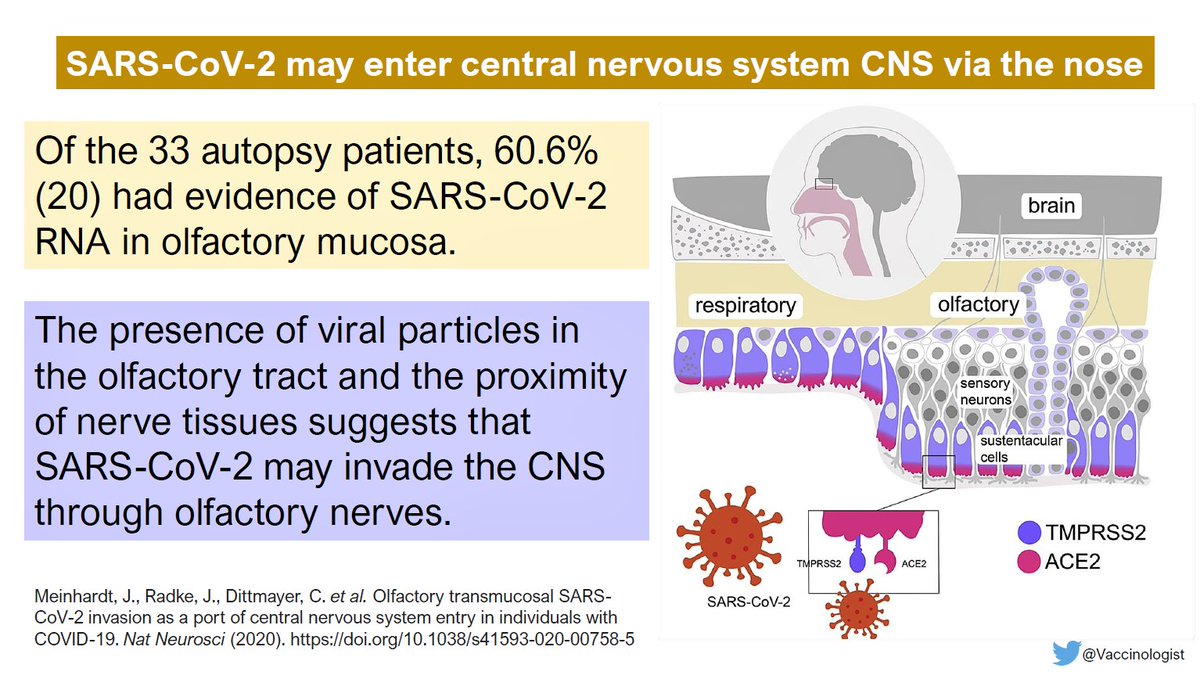
También pueden afectar a las funciones hepática y renal, provocando que algunos pacientes deban ser dializados durante su estancia hospitalaria. En algunos casos también se llegó a desarrollar prostatitis (ver artículo). Se cree que algunos de los pacientes que experimentan dolores de cabeza intensos podrían sufrir encefalitis, que muchas veces provoca epilepsias o problemas de tipo psiquiátrico, como comportamientos violentos. Incluso se ha estudiado la posibilidad de que pudieran surgir crisis epilépticas de novo sin episodios previos conocidos (ver noticia). De hecho, se ha observado que más de la mitad de los pacientes ingresados en España han desarrollado diversos problemas neurológicos, de muy diverso tipo (ver noticia). Entre los más comunes están los dolores musculares de origen nervioso (mialgias), cefaleas, mareos, trastornos de la conciencia, insomnio, ansiedad, psicosis, aunque también, en menor proporción, se han detectado problemas neuromusculares (miopatías), disautonomía, convulsiones, etc. Las complicaciones de este tipo fueron la causa del 4% de fallecidos por COVID-19 según estos estudios. Un estudio publicado en Nature Neuroscience, en base a unas autopsias realizadas, sugerían que el SARS-CoV-2 podría adentrarse en el Sistema Nervioso Central a través de las mucosas nasales, dado que se demostró la presencia del virus en estas estructuras nasales y en el cerebro, lo que podría explicar el gran abanico de síntomas de tipo neurológico relacionados con la enfermedad (ver estudio). En febrero de 2021, un estudio señalaba que el virus puede infectar al páncreas a través de las células beta, provocando cambios funcionales en la expresión de insulina estimulada por glucosa, lo que podía llevar a posibles alteraciones metabólicas (ver estudio).
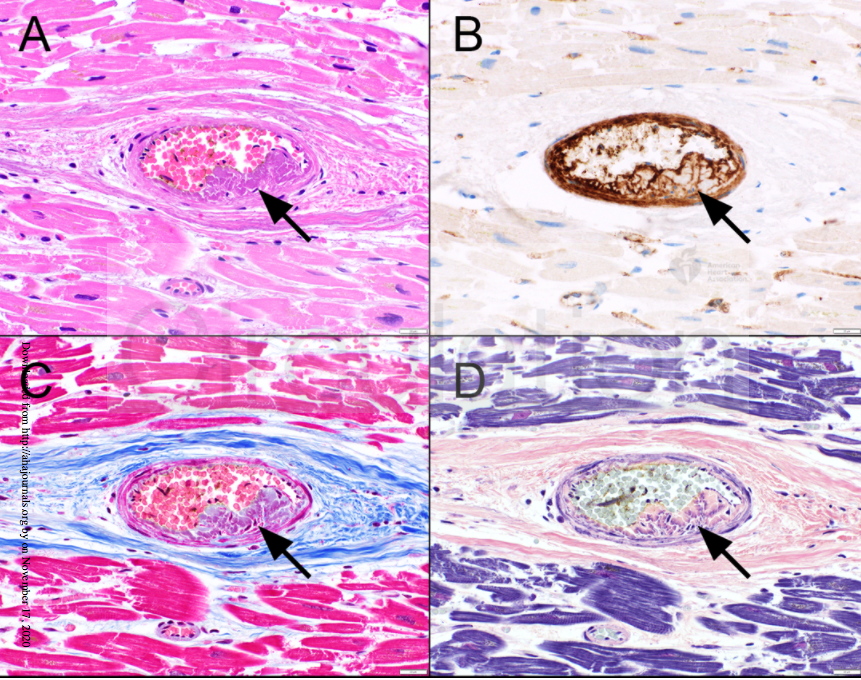
Un equipo de la Universidad Johns Hopkins también publicó un estudio según el cual se detectó importante carga vírica en el oído medio e interno de los pacientes (ver noticia), pudiendo provocar también otitis media o aguda. Y con las primeras autopsias en Italia, se descubrió que en los fallecidos con neumonías bilaterales había microcoágulos sanguíneos a nivel de los alveolos pulmonares (Ver noticia). Parece claro ahora que la COVID-19 provoca coagulopatías que podrían afectar a varios órganos según la gravedad de los casos. Las coagulopatías también se detectaron en Nueva York (ver noticia), donde se observó que las máquinas de diálisis de los pacientes con afectación renal dejaban de funcionar por los microcoágulos que se formaban, que atascaban el circuito. Además, como se ha comentado, los pacientes suelen presentar valores anormales del factor de coagulación Dímero-D en las analíticas sanguíneas. Por tanto, pese a que el virus se pensaba que era principalmente respiratorio, parece ser que provoca daños de distinta consideración en todo el organismo como consecuencia de las coagulopatías que provoca. Y este hecho cobra especial relevancia con respecto a las secuencias a corto/medio plazo que se van descubriendo, y que se comentan a continuación. Otros estudios realizados confirman las coagulopatías: un estudio sobre varias autopsias concluyó que el 42% de los casos se hallaron trombos no detectados (ver noticia), y otro estudio del Hospital Gregorio Marañón de Madrid confirmó que el 15% de los pacientes ingresados tenían trombosis venosas asintomáticas (ver noticia). Otro estudio más encontró evidencias de microtrombos de fibrina y miocarditis en un número destacable de autopsias (ver estudio).
Un estudio publicado en Nature mostró además, como hallazgos significativos, que los pacientes más graves presentaban un mayor nivel de citoquinas proinflamatorias (IFN-α, IFN-γ, TNF-α, IL-1βy IL-18), así como una mayor persistencia de la carga viral (ver estudio). Por tanto, se sabe que los pacientes más graves tienen 3 características comunes, que son una mala o deficiente actividad del interferón en su organismo, una persistente presencia de carga viral en sangre, y una respuesta inflamatoria exacerbada causada por la tormenta de citoquinas.
En julio de 2020, un estudio realizado entre 1.653 pacientes, llevado a cabo por el King's College de Londres, clasificó en seis grupos los diferentes síntomas del coronavirus (ver estudio). En todos esos grupos había síntomas comunes, como dolores de cabeza, y la pérdida de olfato y gusto. Dichos grupos según la sintomatología serían los siguientes:
- Grupo 1: Fue el grupo más numeroso (462 pacientes). Los síntomas se centran en el tracto respiratorio superior, e incluyen tos persistente y dolor muscular. Solo el 1,5% necesitó asistencia respiratoria.
- Grupo 2: Los síntomas se centran en el tracto respiratorio superior, pero se añaden fiebre y pérdida de apetito. El 4,4% de ellos necesitó asistencia respiratoria. Este grupo, junto con el grupo 1, conformaron el grupo de pacientes que mostraron un desarrollo más leve de la enfermedad.
- Grupo 3: este es un grupo con pocos síntomas, principalmente de tipo gastrointestinal, como la diarrea. El 3,7% de ellos necesitó asistencia respiratoria.
- Grupo 4: aquí los pacientes experimentaban de manera temprana fatiga severa, dolor torácico continuo y tos. El 8.6% necesitó asistencia respiratoria.
- Grupo 5: los síntomas en este grupo incluyen confusión, pérdida de apetito y fatiga severa. De ellos, el 9.9% necesitó asistencia respiratoria.
- Grupo 6: este era el grupo menos numeroso (167 pacientes). El principal síntoma es una gran dificultad respiratoria, así como dolor torácico, confusión, fatiga y diarrea. El 20% de ellos necesitó asistencia respiratoria.
En agosto, un nuevo estudio publicado en The Lancet a partir de 10 autopsias en pacientes graves, encontró cuatro procesos patológicos dominantes: trombosis en algún órgano (principalmente pulmones, y también en muchos casos en corazón y riñón), daño renal, hemofagocitosis y linfopenia. También se observó en menor proporción pancreatitis, pericarditis, disección aórtica, o endocarditis (ver estudio).
En Inglaterra se observó un síndrome inflamatorio similar a la enfermedad de Kawasaki. Sin embargo, un estudio del Imperial College de Londres demostró que, a pesar de los síntomas, estos niños no tenían dicha enfermedad, sino una nueva patología con la misma sintomatología, que se ha denominado Síndrome Multisistémico Inflamatorio Pediátrico Temporalmente Asociado con el SARS-CoV-2- (PIMS-TS o MIS-C), tras un estudio con 58 niños ingresados en hospitales de Inglaterra. Aunque es rara y poco frecuente, existe preocupación sobre sus posibles daños a largo plazo, si bien en la mayoría de casos ya se han recuperado. Si bien no se puede afirmar con rotundidad que sea provocado por la COVID-19, sí que es cierto que 45 de los 58 niños estudiados tenían anticuerpos específicos contra el SARS-CoV-2, lo que induce a pensar que puede haber una relación directa (ver noticia). Tras meses de investigación urgente, se ha conseguido identificar como signos tempranos la fiebre, las erupciones cutáneas, el dolor abdominal, la diarrea y los vómitos, y puede desencadenar una inflamación grave en cuestión de horas, requiriendo por lo general cuidados intensivos (se estima en un 70% de casos) y en algunos casos, provocar la muerte. Un informe del CDC de los EEUU incluso señala que la mayoría de muertes en menores de 21 años eran debidas a este síndrome (ver noticia). Al parecer, el MIS-C se desarrolla generalmente varias semanas después de que aparezcan los síntomas clásicos del virus en niños, como tos, dolores musculares o congestión, e incluso podría darse después de una infección asintomática en algunos casos, lo cual parece especialmente delicado porque podría desarrollarse incluso sin saber que el niño ha estado infectado, lo que dificultaría el diagnóstico precoz. Al parecer, el virus podría replicarse en el aparato digestivo en los niños, según estudios.
No obstante, y aunque cada vez se conoce más sobre el SARS-CoV-2, si algo ha demostrado este virus es que es extremadamente impredecible. Así, podemos encontrar casos poco frecuentes pero sorprendentes, como el de una mujer asintomática que casi pierde la vida súbitamente a causa del virus (ver noticia).
Pese a que el virus inicialmente se pensaba que era respiratorio, estudios recientes sugieren que las complicaciones pulmonares son finalmente resultado de una alteración de los vasos sanguíneos (ver estudio publicado en Nature). La clave sería el endotelio, que es un tejido que tapiza el interior de los vasos sanguíneos, y que además de ese recubrimiento, intervienen en procesos como por ejemplo el intercambio de nutrientes y sustancias de desecho con las células del cuerpo. También evita la formación de coágulos sanguíneos. La disfunción endotelial es responsable de numerosas enfermedades (arteriosclerosis, isquemias, hipertensión arterial, sepsis, trombosis, vasculitis, hemorragias, etc). A nivel pulmonar, se cree que el SARS-CoV-2 provoca un edema tisular (acumulación de líquido en los pulmones), inflamación del endotelio (endotelitis), activación de las vías de coagulación, e infiltración descontrolada de células inflamatorias.
El primer estudio que sugería que el SARS-CoV-2 infectaba las células endoteliales fue publicado en marzo por investigadores suizos, en la revista The Lancet (ver estudio). No se veía clara la relación entre una posible infección respiratoria con otra sintomatología que afectaba a otros órganos vitales, así como la formación de trombos. Observando al microscopio tejidos de pacientes fallecidos, comprobaron que el virus había infectado a las células endoteliales de los mismos, provocando la inflamación del tejido respiratorio, pero también del endotelio de otros órganos. De hecho, en las autopsias se encontraron grandes cantidades del virus en los órganos de los fallecidos (ver artículo).
Posteriormente, más investigaciones han detectado patrones similares, por lo que los efectos del virus sobre el endotelio explicarían la gravedad de los casos, especialmente, en pacientes que no son población de riesgo, de quienes se cree que podrían sufrir algún trastorno endotelial o vascular de base no diagnosticado, lo cual podría amplificar los efectos de la infección. Así, el investigador belga Peter Carmeliet, elaboró una hipótesis de cómo el coronavirus SARS-CoV-2 atacaría al endotelio, desencadenando un fallo en distintos órganos:
- Cuando se produce la infección, el virus se une al receptor ACE2 infectando células endoteliales de los capilares pulmonares, afectando al endotelio, y aumentando la permeabilidad vascular, promoviendo la aparición de un edema pulmonar que conduce a una insuficiencia respiratoria.
- Después, los glóbulos blancos se dirigen hacia ese endotelio pulmonar, y el sistema inmunológico comenzaría a enviar gran cantidad de células para atacar a la infección, incrementando el daño producido sobre las células del tejido muscular, y pudiendo producirse en esta fase un proceso denominado apoptosis, por el cual algunas células mueren.
- Los daños directos sobre el endotelio provocarían otras consecuencias graves, como sería la alteración de las uniones entre las células endoteliales, lo cual desencadenaría una coagulación sanguínea incontrolada. Por otra parte, la obstrucción de los capilares pequeños por las células inflamatorias, unido a la posible aparición de trombos en vasos más grandes, provocaría isquemias (disminución del riego sanguíneo) en el tejido pulmonar, e incluso dar origen a la “tormenta de citoquinas”.
- Otro estudio tuvo como hallazgo significativo que la subunidad 2 de la proteína espiga, podrían unirse a los receptores ACE2 de células endoteliales, y podían causar la desestabilización de la barrera hematoencefálica (que es una barrera compuesta de células de alta densidad que restringen el paso de sustancias del torrente sanguíneo mucho más de lo que lo hacen las células endoteliales capilares en otras partes del cuerpo) en regiones cerebrales clave, de modo que esta barrera, que normalmente mantiene a los agentes nocivos fuera del cerebro, se vería desestabilizada, y podría darse una neuroinvasión por parte del virus, lo que explicaría las manifestaciones neurológicas experimentadas por los pacientes de COVID-19 (ver artículo). Un estudio publicado en diciembre de 2020 confirmaba que el la proteína S1 del virus había superado esta barrera hematoencefálica con facilidad al ser suministrada por vía intravenosa a ratones, y también al ser suministrada intranasalmente, aunque con más limitaciones (ver estudio).
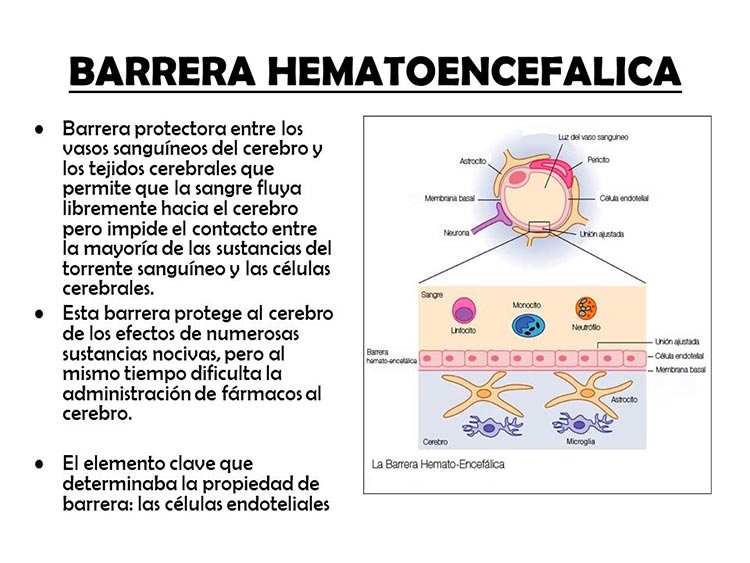
Fuente: fantasymundo
- Otro estudio de abril de 2021 publicado en la revista Brain concluía sin embargo que, a pesar del daño cerebral, el virus no sería capaz de infectar al cerebro, pero causaría daños al mismo por la hipoxia generada como consecuencia de la afectación pulmonar o por la inflamación generada en vasos sanguíneos del cerebro. Según los investigadores del mismo, no se pudo encontrar ningún signo de virus dentro de las células cerebrales de más de 40 pacientes con COVID-19, pero si observaron muchos cambios patológicos en estos cerebros, lo que podría explicar por qué los pacientes gravemente enfermos experimentan confusión y delirio y otros efectos neurológicos graves, y por qué aquellos con casos leves pueden experimentar niebla cerebral durante semanas y meses. El estudio examinó los cerebros de 41 pacientes con COVID-19 que sucumbieron a la enfermedad durante su hospitalización. Los pacientes tenían edades comprendidas entre los 38 y los 97 años; aproximadamente la mitad habían sido intubados y todos tenían daño pulmonar causado por el virus. Tampoco encontraron virus en el bulbo olfatorio. aunque sí se encontró ARN viral y proteínas en la mucosa nasal de los pacientes y en la mucosa olfativa en la parte alta de la cavidad nasal. Se encontraron una gran cantidad de áreas dañadas por la falta de oxígeno, lo cual era de prever pues todos padecieron enfermedad pulmonar grave. Los investigadores creen pequeñas áreas de daño hipóxico fueron causadas por coágulos de sangre, comunes en pacientes con COVID-19 grave, que detuvieron temporalmente el suministro de oxígeno a esa área. Otro hallazgo más sorprendente fue la gran cantidad de microglía activada que encontraron en el cerebro de la mayoría de los pacientes (las microglías son células del sistema inmunitario de cerebro). La microglía activada, que provoca la pérdida de neuronas de forma permanente, se encontró sobre todo en la parte del encéfalo que regula el ritmo cardíaco y el respiratorio, y los niveles de conciencia, y también en el hipocampo, que afecta a la memoria y el estado de ánimo (ver estudio).
La afectación al endotelio podría explicar también por qué la diabetes, la hipertensión arterial y la obesidad constituyen un importante factor de riesgo, ya que en estos tres casos, el endotelio está dañado. En la siguiente imagen, extraída de una publicación en la revista European Heart Jornal (ver publicación), puedes ver la diferencia entre un endotelio sano (izquierda) y un endotelio dañado (derecha), así como las consecuencias que puede tener, incluyendo trombosis pulmonar, miocarditis, ictus, trombosis, y daño renal.

Fuente: European Heart Journal
En diciembre, un estudio publicado concluyó que los pacientes inmunodeprimidos podrían tardar en eliminar el virus varias semanas, cultivándose virus viable hasta dos meses después de la infección. Esto, además de ser compatible con un virus persistente, podría hacer revisar las pautas actuales de aislamiento en este tipo de pacientes, pues podrían ser contagiosos durante mucho más tiempo (ver estudio).
En la siguiente infografía se puede ver, de manera aproximada, la evolución de casos y sus porcentajes. El 50% de las personas no tendrían síntomas, el 40% se recuperarían en 10 o 14 días tras la aparición de síntomas, el 8'5% requerirían hospitalización, recuperándose tras una o dos semanas desde el ingreso, y el 1'5% necesitarían cuidados intensivos, resultando el porcentaje de fallecidos entre el 0'75% y el 1%.
Sin embargo, esta infografía no recoge los porcentajes de pacientes con secuelas tras la infección, datos que parecen estar menos claros. Finalmente, las principales causas de fallecimiento por COVID parecen ser:
- Hipoxia silenciosa: una de las causas principales de muerte por COVID es la falta de acceso a oxígeno, cosa que ha sucedido en casas y en los hospitales. El virus desconecta las alertas del organismo ante una falta de oxigenación, de forma que el paciente puede pasar días sin oxigenación adecuada, sin dificultad respiratoria, pero con daño orgánico progresivo. Esto supone un deterioro silencioso del organismo, y la falta de una respuesta médica temprana, por lo que es recomendable tener un pulsioxímetro en casa para poder detectar cuando baja oxigenación. Si es menor de 92% o baja más de 4% la saturación habitual, no hay que dudar en pedir ayuda médica.
- Procesos trombóticos: esta es una complicación grave en determinados pacientes, como aquellos con obesidad mórbida, diabetes, hipertensión no controlada, y otras enfermedades crónicas. El virus afecta al endotelio, provocando la formación de microtrombos o microcoágulos en tejidos vitales como pueden ser cerebro, corazón, pulmones, riñones, etc. Un estudio publicado en abril de 2021 sugiere que la infección por SARS-CoV-2 induce un proceso conocido como inmunotrombosis, en el que los neutrófilos y monocitos activados interactúan con las plaquetas, lo que lleva a la formación de coágulos intravasculares en vasos pequeños y grandes. Las complicaciones microtrombóticas pueden contribuir al síndrome de dificultad respiratoria aguda (SDRA) y otras disfunciones orgánicas. Por tanto, pueden resultar útiles las estrategias terapéuticas destinadas a reducir la inmunotrombosis. Se han propuesto varios fármacos antitrombóticos e inmunomoduladores como candidatos para tratar pacientes con infección por SARS-CoV-2 (ver estudio).
- La tormenta de citoquinas: esta inflamación desenfrenada es causada por una reacción tardía y exagerada del sistema inmune, que cursa con malestar, fatiga, fiebre prolongada, elevación de proteína C reactiva, valores altos de ferritina, elevado dímero-D... Además, esto afecta también al propio sistema inmune, provocando que los linfocitos pierdan su capacidad para matar células infectadas y producir anticuerpos neutralizantes del virus.s neutralizantes.
Otro aspecto notablemente preocupante es que los efectos sobre la salud del Covid-19 no solo pueden extenderse durante meses, sino que parecen aumentar el riesgo de muerte y afecciones médicas crónicas, incluso en personas que nunca estuvieron lo suficientemente enfermas como para ser hospitalizadas. En un estudio publicado en Nature (ver estudio) en abril de 2021, en el que varios investigadores analizaron los registros médicos de más de 73.000 personas en los Estados Unidos cuyas infecciones por coronavirus no requirieron hospitalización, se concluía que entre uno y seis meses después de infectarse, esos pacientes tenían un riesgo de muerte significativamente mayor (60 por ciento más alto) que las personas que no habían sido infectadas con el virus.




 Factores de riesgo
Factores de riesgo Técnicas de detección
Técnicas de detección Tratamientos
Tratamientos Vacunas
Vacunas Carga viral
Carga viral Mutaciones
Mutaciones Letalidad y mortalidad
Letalidad y mortalidad Prevención: mascarillas
Prevención: mascarillas Prevención: Ventilación y filtración (HEPA)
Prevención: Ventilación y filtración (HEPA) Otras medidas de prevención
Otras medidas de prevención Impacto de la pandemia
Impacto de la pandemia Fin de la pandemia
Fin de la pandemia Prevención en centros educativos
Prevención en centros educativos Enlaces de interés
Enlaces de interés





