Última actualización: 26 de abril de 2021
En general, los virus son pequeños organismos infecciosos que necesitan invadir una célula para replicarse. Los virus penetran en una célula del organismo del individuo infectado (llamada célula huésped), liberando su material genético interno (que puede ser ADN o ARN). Este material genético toma el control de la célula, obligándole a hacer copias del virus. Por lo general, las células infectadas mueren, dado que los virus les impiden realizar sus funciones normales, pero antes de que eso suceda, liberan nuevas copias del virus listas para invadir otras células.
Todos los coronavirus presentan una cadena ARN en su interior, envueltos en una bicapa lipídica esférica, y contiene cuatro proteínas estructurales, tres de ellas en la membrana.
En concreto, el SARS-CoV-2 contiene ARN con casi 30.000 nucleótidos, empaquetado con un tipo de proteína, todo ello dentro de una capa lipídica en la que tiene tres tipos de proteínas estructurales: la proteína espiga S, la proteína E, la proteína M (membrana) y la proteína N que es la proteína estructural que se encuentra en el interior (nucleocápside). Además de estas proteínas, su ARN contiene información para generar dos proteínas grandes, denominadas ORF1a y ORF1b, que se traducen en la enzima polimerasa vírica (RdRp), y tiene otras proteínas accesorias, que podrían jugar un papel fundamental para la adaptación del virus a hospedadores específicos.

Mapa del genoma ARN del coronavirus SARS-CoV-2 convertido a ADN, Fuente: Naukas
La denominada proteína espiga de la membrana (spike glycoprotein) se une a unos receptores de las membranas de las células humanas llamados ACE2, atacando así a nuestro organismo. Ambas se unen y esto supone una puerta de entrada al ARN vírico, que se duplica en el interior de las células humanas y se producen réplicas del virus dispuestas a atacar otras células (ver noticia). En este artículo de la revista Investigación y Ciencia puedes consultar una infografía muy interesante acerca de cómo se produce el ataque y la respuesta del organismo. Otros virus, como los causantes del SARS y el MERS, también utilizaban los receptores ACE2 de las células como puerta de entrada a las mismas.

Fuente: commons.wikimedia.org
La RdRp o enzima ARN replicasa, es una enzima propia de los virus que cataliza la replicación del ARN. Cuando el virus consigue insertar su ARN en el interior de la célula, los ribosomas, orgánulos de las células que se encargan de sintetizar proteínas a partir de ARN, traducen el ARN del virus y sintetizarán las proteínas ORF1a y ORF1b que forman la RdRp. Esta enzima entonces se encargará de replicar el ARN del virus, de forma que finalmente se conseguirá liberar al medio externo de la célula nuevas réplicas del virus que infectarán nuevas células.
La proteína espiga está divida en dos subunidades. La subunidad 1 es la parte mediante la cual el virus se une a una célula para infectarla. Una zona invariable entre las distintas cepas en esta subunidad sería útil de cara a desarrollar una vacuna. La subunidad 2 es la zona que se une a la envuelta del virus.

Fuente: Rica
En octubre, un estudio publicado en la revista Science ampliaba el conocimiento que se tenía hasta ese momento sobre el mecanismo de entrada del virus a las células humanas. Investigadores liderados por la Universidad de Bristol, Reino Unido, localizaron una nueva "cerradura" por la que el virus podía entrar a las células: la proteína neuropilina-1 o NRP1, sería reconocida por la proteína espiga del virus, y así podría entrar en la célula. Esto hace que el SARS-CoV-2 sea altamente infeccioso y capaz de propagarse rápidamente en las células humanas. Además, se consiguió mediante el uso de anticuerpos monoclonales bloquear esa interacción, reduciendo así la capacidad del virus para infectar las células. Es decir, este descubrimiento podría tener un importante valor de cara a posibles tratamientos de la enfermedad. Científicos de la Universidad Técnica de Múnich (Alemania) y la Universidad de Helsinki (Finlandia), descubrieron también, de forma independiente, que la neuropilina-1 facilita la entrada e infectividad de las células del SARS-CoV-2. Se cree que esta proteína jugaría un papel importante para la infección, incluso más que los receptores ACE-2. Esta proteína se encuentra principalmente en la capa celular de la cavidad nasal (y también en células pulmonares), por lo que la pérdida de olfato podría estar relacionada con la presencia de esta proteína en estos tejidos (que además tienen pocos receptores ACE2); de hecho, en muestras de pacientes fallecidos, se pudo comprobar que las células que tenían esta proteína estaban realmente infectadas por el virus.
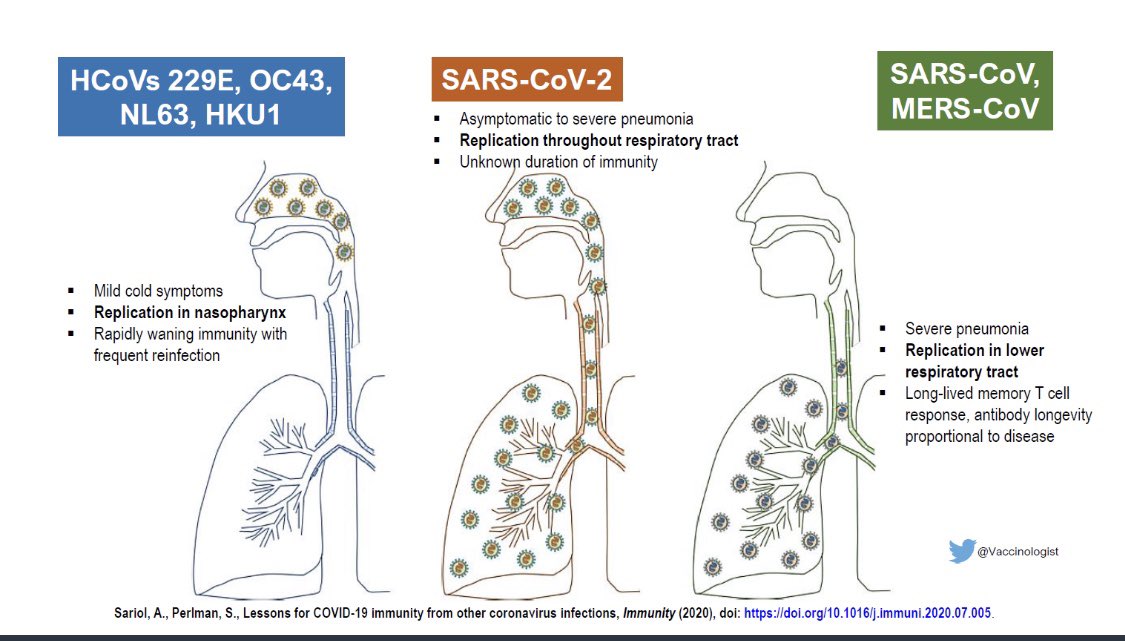
Con respecto a dónde se replica el virus, hay estudios que muestran que se puede replicar en todo el tracto respiratorio, tanto superior (fosas nasales, boca, faringe, laringe) como en el inferior (tráquea, bronquios, bronquiolos, pulmones). Esto lo hace diferente de los otros tipos de coronavirus, ya que los más leves afectan solo al tracto superior, y los más graves conocidos con anterioridad, los que provocan SARS y MERS, afectaban al tracto respiratorio inferior.
En el siguiente vídeo, extraído de la web de National Geographic (ver web), puedes ver una explicación de cómo podría atacar el virus al tracto respiratorio una vez que llega a los alveolos pulmonares.
Según el Centro de Control de Enfermedades de EEUU, para que se desarrolle la enfermedad debería producirse un contagio a partir de al menos 1000 partículas virales aproximadamente, por lo que esta cantidad se considera la carga viral necesaria para enfermar (ver noticia). Pero en abril de 2021, un nuevo estudio, al sintetizar los datos disponibles de los eventos de propagación en interiores, estimó una dosis infecciosa de tan solo 10 viriones transmitidos por aerosoles (ver estudio).
En diciembre, un estudio preliminar apuntaba a que el virus podría "esconderse", al menos parcialmente, en un lugar inesperado: los cromosomas de las células humanas. Al estilo de lo que pueden hacer el virus del VIH y otros retrovirus, podrían integrar algunas partes de su código genético en el ADN de la cromatina celular, lo que podría tener profundas implicaciones de confirmarse, como falsas señales de infección activa hasta resultados engañosos de estudios con tratamientos. Dicho estudio mostraba una integración de código del ARN del virus en ADN en una placa de laboratorio, si bien también citaba datos de secuencia publicados en infecciones humanas, que sugieren que esto podría haber sucedido. Los autores del artículo resaltaban que esto no tiene por qué implicar que el virus quede permanentemente en nuestras células con la capacidad de producir nuevas copias, como sí hace el VIH, pero es algo que debe estudiarse más en profundidad, según algunos científicos. Quizás esto podría ser la causa para algunos de que, en algunos pacientes, después de la recuperación, siguieran dando positivo en la PCR.
Para probar que el genoma del ARN del SARS-CoV-2 podría integrarse en el ADN, los investigadores agregaron el gen de una enzima denominada transcriptasa inversa, que es capaz de convertir una cadena de ARN en una cadena de ADN equivalente, y también usando secuencias de ADN humano conocidas como elementos LINE-1, que son restos de antiguas infecciones retrovirales y que constituyen el 17% aproximadamente del genoma humano. De esta forma, algunos trozos de ARN se integraban en los cromosomas humanos (ver estudio). Es por ello que si las secuencias de LINE-1 pueden producir RT de forma natural en las células humanas, la integración del código del virus podría ocurrir en personas infectadas, o coinfectadas por SARS-CoV-2 y VIH. Sin embargo, aun no esta claro si estas integraciones permanecen durante mucho tiempo o mueren.
:quality(85)//cloudfront-us-east-1.images.arcpublishing.com/infobae/B2JA43MXKJEBRCK5XIR5WOBOOE.jpg)
Imagen del SARS-CoV-2. Fuente: Sai Li, Tsinghua University School of Life Sciences
¿CÓMO SE DEFIENDE NUESTRO ORGANISMO?
Nuestro organismo goza de un sistema inmunológico que nos protege frente a infecciones de agentes patógenos (también denominados antígenos). Dicho sistema se divide en dos partes:
- Sistema inmunitario innato: proporciona la llamada inmunidad innata, y está formado por células y mecanismos que nos defienden frente a agentes patógenos de forma inespecífica (es decir, de forma general, independientemente del patógeno que pretenda atacar a nuestro organismo). Se trata por tanto de un mecanismo de defensa genérico, que además, no proporciona inmunidad protectora a largo plazo, sino que supone una defensa inmediata contra la infección. Dentro de este sistema podemos encontrar distintos tipos de barreras:
Las barreras primarias son aquellas que tratan de evitar la entrada de un patógeno invasor (piel, mucosas, lágrimas, cilios de las vías respiratorias, saliva, flora intestinal,...)
Las barreras secundarias son aquellas que luchan contra un patógeno que ya ha entrado en el cuerpo (reacción inflamatoria con liberación de histaminas, macrófagos, células NK o asesinas naturales, interferón,...).
- Respuesta inmunitaria adaptativa: son las barreras terciarias, defensas específicas que se producen por el organismo cuando la respuesta innata no es eficaz. Al contrario que las barreras primarias y secundarias, que siempre están presentes, estas barreras se desarrollan como respuesta a la invasión de un patógeno concreto, es decir, se estimula su producción tras la exposición a agentes infecciosos, por lo que la respuesta es muy específica y diversa frente a los distintos antígenos que atacan al organismo. Además, consiguen fabricar memoria contra los agentes patógenos, por lo que las respuestas a una infección recurrente de un mismo patógeno suelen ser más rápidas y precisas. Hay dos tipos de respuesta inmunitaria adaptativa:
La inmunidad celular es una forma de respuesta mediada por unas células especiales del sistema inmunológico, llamadas linfocitos T. Supone una defensa contra patógenos como virus o bacterias. Muchos microbios son ingeridos por fagocitos (células de defensa del sistema inmunitario innato que ingieren microbios), pero sobreviven en su interior, y otros (en especial los virus), acaban penetrando en el interior de una célula con el fin de replicarse; una vez que están en estos lugares, los microbios no son accesibles por los anticuerpos que circulan por la sangre, por lo que la inmunidad celular se encarga de defendernos contra los patógenos en esas ubicaciones, ya que fomenta la destrucción de los antígenos residentes en los fagocitos y la eliminación de células infectadas. Cuando se activan los linfocitos T, se generan linfocitos T de memoria para proteger contra posibles reinfecciones futuras.
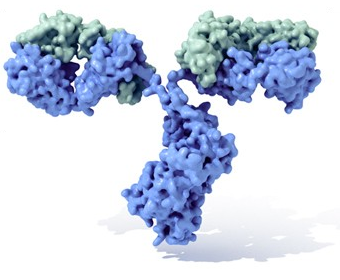
La inmunidad humoral: es el principal mecanismo de defensa contra los antígenos, de forma que los componentes que atacan a los antígenos son macromoléculas, como por ejemplo, los anticuerpos. Esta respuesta es mediada por otro tipo de células, los linfocitos B. Este tipo de linfocitos tiene capacidad para detectar agentes patógenos, y una vez detectados, activar la producción de anticuerpos de defensa (Ig) que se van a unir perfectamente con el patógeno. Cuando nuestra médula ósea produce los linfocitos B, sus genes se van recombinando al azar, de forma que se acaban generando millones de linfocitos B distintos entre sí, con el objetivo de poder reconocer la mayor cantidad de patógenos posible. En alguna ocasión puede ser que estos linfocitos reconozcan estructuras de nuestro propio organismo, pero lo normal es que se detecten y no se les deje madurar para fabricar anticuerpos (aunque algunas veces se producen fallos y se desarrollan las llamadas enfermedades autoinmunes). Cuando entra un antígeno nuevo (como por ejemplo el SARS-CoV-2), puede ser detectado por un linfocito B, y entonces se activa, produciéndose una expansión clonal, es decir, muchas copias de ese linfocito B que ha detectado el virus. Y a su vez, estos linfocitos B empiezan a producir anticuerpos, también denominados inmunoglobulinas, que se clasifican en cinco tipos: IgA, IgD, IgE, IgG e IgM. En primer lugar se producen anticuerpos de tipo IgM, y más tarde, comienza a producir de tipo IgG, más efectivos que los IgM. Pasado un tiempo, también se producen los linfocitos B de memoria, que perdurarán en el tiempo ante posibles reinfecciones, actuando de modo más rápido y eficaz, siempre y cuando no se produzcan mutaciones en el virus que lo hagan irreconocible.
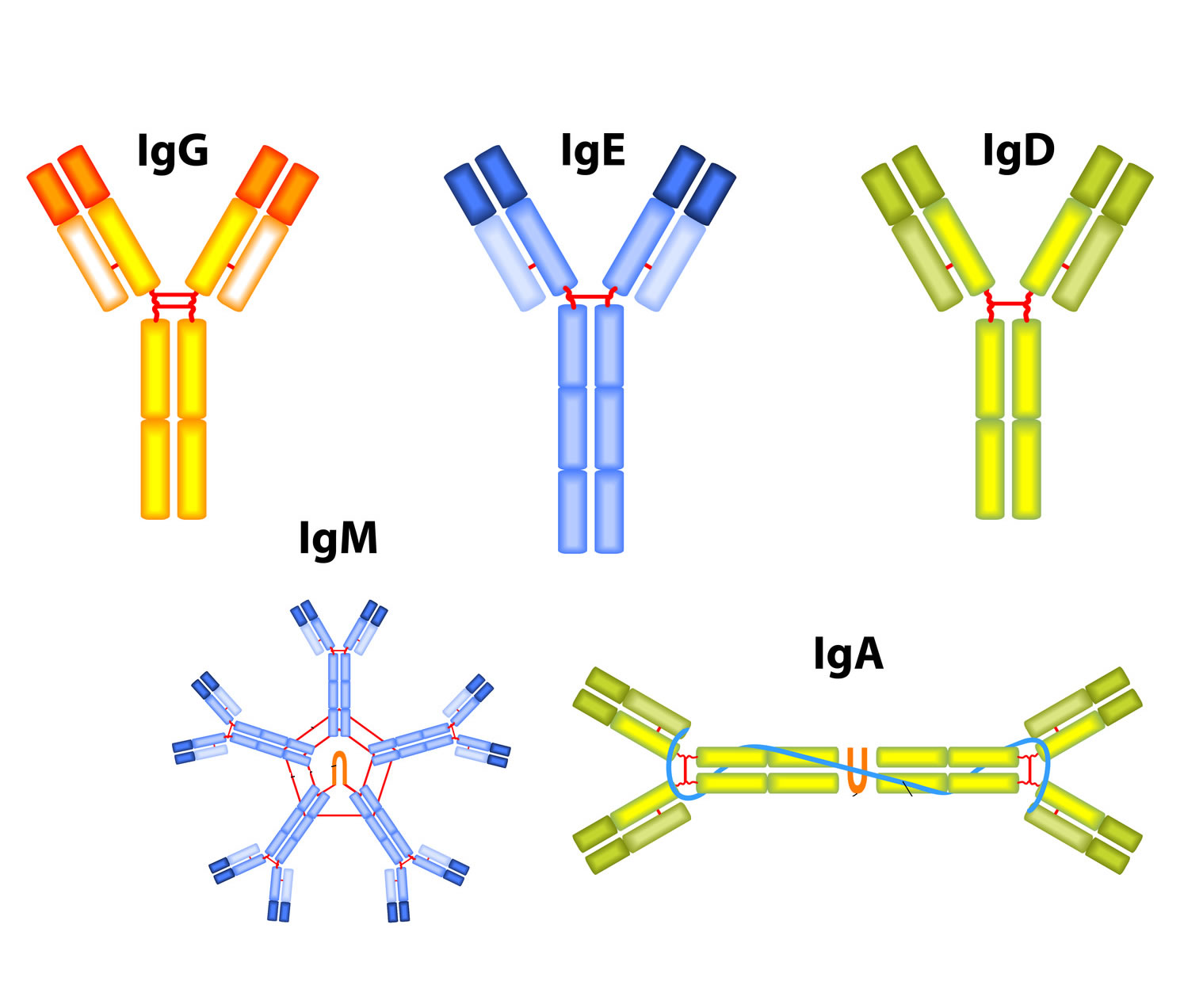
Fuente: definicionabc.com

En la siguiente imagen puedes ver un resumen de cómo funciona la protección del sistema inmunológico; cuando un virus entra en el organismo y empieza a replicarse, entran en juego unas células de presentación de antígeno. Estas células detectan el patógeno, y lo fagocitan y digieren, descomponiéndolo en muchos fragmentos diferentes. Estos fragmentos se transportan a la superficie de la misma célula, y se "presentan" a los linfocitos T CD4+. A partir de ahí, median la respuesta a través de células asesinas T CD8+, y también mediante linfocitos B, que empiezan a fabricar anticuerpos (Ig) que impiden la interacción del patógeno con las células, de forma que este patógeno al final es destruido por fagocitos mediante opsonización.
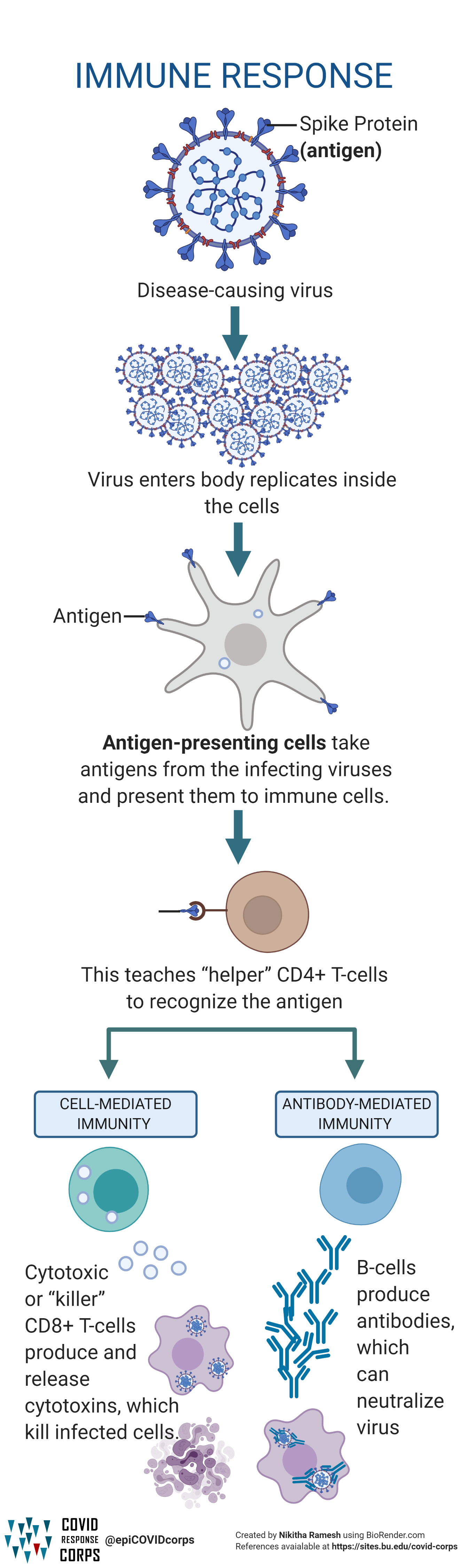
En el caso concreto del SARS-CoV-2, como ya hemos comentado, se sabe que el organismo genera anticuerpos específicos, que atacan al SARS-CoV-2, de tipo IgM e IgG (y dentro de ellos hay varios subtipos distintos de anticuerpos), y que también puede acabar desarrollando unas defensas especiales, las llamadas células de memoria, que se forman después de la infección primaria, y cuya misión es generar una respuesta inmunitaria mediada por anticuerpos más robusta y acelerada en el caso de reinfección. Las vacunas otorgan a nuestro sistema inmunológico lo que se denomina inmunidad artificial.
Bien es cierto que no siempre se generan anticuerpos IgM o IgG. Puede ser que en algunos casos, haya una infección y sea combatida de forma efectiva por el sistema inmune innato, por lo que no sería precisa la acción de los linfocitos B. O puede que incluso en algunos organismos, no haya linfocitos B que reaccionen con el SARS-CoV-2, provocando esto que no se active la producción de IgG o IgM. Algunos estudios hablan de que los producen el 99% de los infectados (ver noticia). Sin embargo, un estudio más reducido encontró pocos anticuerpos en 29 de 111 casos estudiados, un 26% (ver artículo).
Aunque tanto la presencia de anticuerpos neutralizantes y de células T se han relacionado con la resolución de la enfermedad, poco se sabe acerca de las características de los anticuerpos que son fundamentales para una protección contra el virus. Un estudio publicado el 30 de julio en la revista Cell no detectó diferencias significativas entre los anticuerpos IgG o IgA generados por pacientes que habían sobrevivido y por pacientes que habían fallecido, pero sí que se encontraron sutiles diferencias en la respuesta de anticuerpos IgM, mostrándose mayor cantidad de IgM que se asocian a la proteína espiga (S) del virus, y mayor cantidad de anticuerpos IgM que se asocian a la proteína de la nucleocápiside (N) del virus (ver estudio).
Un artículo publicado en septiembre indica que la respuesta inmune comenzaría entre 7 o 10 días después de la infección, detectándose una robusta expansión del plasmablasto a partir de entonces, apareciendo células B de memoria, y anticuerpos IgM e IgA, para posteriormente ir disminuyendo y dejar paso a anticuerpos IgG. Casi al mismo tiempo se activan los linfocitos T CD4 específicos y los CD8. Se han identificado CD4+ específicos en hasta el 100% de los pacientes recuperados, y CD8+ en aproximadamente el 70%. Con el paso de semanas e incluso meses, permanecen detectables en niveles bajos (ver artículo).

Otro papel importante en la defensa de organismo, aunque más desconocido por ahora, es que pueden jugar las mucosas, que constituyen el componente más grande de todo el sistema inmunológico, habiendo evolucionado para brindar protección en los principales sitios de amenaza de infección. Así, algunos estudios sugieren que como el SARS-CoV-2 puede infectar inicialmente el tracto respiratorio superior, sus primeras interacciones con el sistema inmunológico deberían ocurrir predominantemente en las superficies de la mucosa respiratoria, durante las fases inductiva y efectora de la respuesta. Sin embargo, casi todos los estudios de la respuesta inmune en COVID-19 se han centrado exclusivamente en los anticuerpos séricos y la inmunidad mediada por células, incluidas las respuestas innatas, pero algunos estudios indican que las mucosas pueden tener un papel relevante, incluyendo los anticuerpos de tipo IgA (anticuerpos que se encuentran en mayor concentración en las mucosas). Así, un estudio publicado a finales de noviembre reclamaba por así decirlo más atención al papel que jugaban las mucosas, recomendando estudios adicionales para determinar su puede jugar un papel determinante en la infección asintomática o presintomática, y los casos leves y moderados de enfermedad COVID-19. Además, los autores señalan que las respuestas inmunitarias de las mucosas pueden variar según los diferentes grupos de edad y poblaciones (ver estudio).
En los casos más graves de la COVID-19 se observó un fenómeno denominado tormenta de citoquinas (ver artículo sobre tormenta de citoquinas).. Las citoquinas o citocinas son moléculas proteicas formadas principalmente por macrófagos (como parte del la respuesta inmunitaria innata), o por linfocitos T (como parte de la respuesta inmunitaria adquirida). Son moléculas que actúan mediando interacciones entre células del sistema inmunológico, y su producción es relativamente transitoria, durante una infección. Pero en algunos casos, las citoquinas, se descontrolan, como parte de una respuesta inmunitaria desproporcionada ante un patógeno altamente peligroso, afectando a distintos órganos y sistemas del cuerpo, en especial, a los pulmones en el caso del SARS-CoV-2, pudiendo llegar a obstruir las vías respiratorias y provocar el fallecimiento. Los síntomas de una tormenta de citoquinas incluyen fiebre, fatiga y náuseas. Se cree que la tormenta de citoquinas fue la causante de un gran número de fallecimientos durante la pandemia de la mal llamada gripe española (1918), e incluso, de la epidemia de SARS (2003), y de la gripe aviar.

Cuando respiramos, tomamos oxígeno del aire, y este llega a unas zonas de los pulmones denominadas alveolos pulmonares. En los alveolos, el oxígeno pasa a la sangre, y esta distribuye el oxígeno a todas las células del organismo, pues es esencial para su funcionamiento. Las células además producen dióxido de carbono como sustancia de desecho, que llega a los alveolos a través del torrente sanguíneo para ser expulsada en la espiración.

Cuando el caso es grave, los alveolos pulmonares, formados por células llamadas neumocitos, se ven atacados por el virus, que penetra en ellas para replicarse, pero también por nuestro sistema inmunológico, que reacciona de manera desproporcionada.
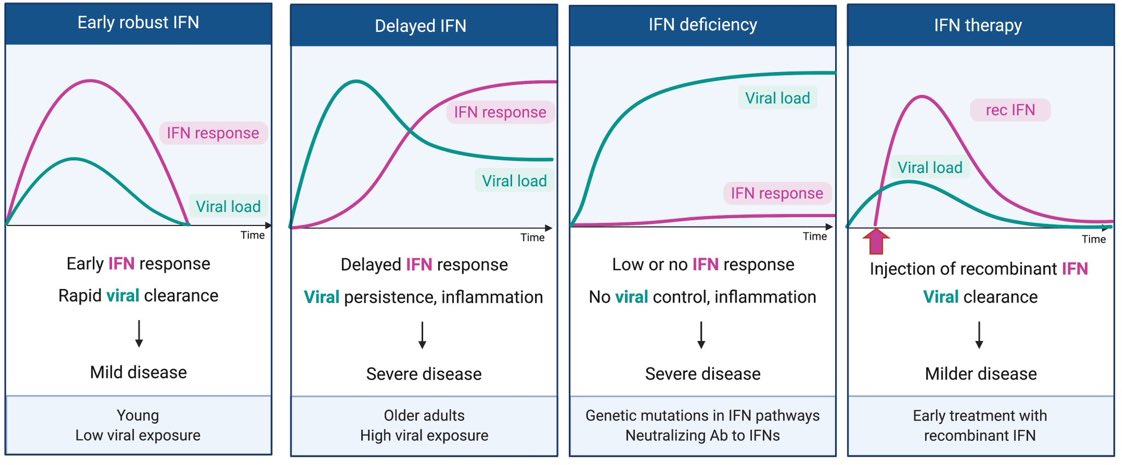
Un estudio publicado en julio en Nature encontró que los pacientes que presentaban una evolución moderada de la enfermedad, presentaba una baja expresión de citoquinas proinflamatorias, lo que ayudaba a la recuperación, pero en los casos más severos, había una gran cantidad de citoquinas proinflamatorias, de forma que muchos de estos pacientes estudiados acabaron falleciendo. Se observó también que los niveles del virus a nivel nasofaríngeo no fueron significativamente distintos en pacientes moderados y graves, pero sí que la carga viral disminuía mucho más lentamente en pacientes en UCI. La carga viral estaba muy relacionada con determinadas citoquinas y con el no control del virus por parte de los interferones, y los pacientes que fallecían tenían niveles altos de interferones y citoquinas, lo que sugiere posibles roles patológicos asociados con estos factores de defensa. (ver estudio). De hecho, en septiembre se conoció un estudio que indica que más del 10% de los enfermos graves producen un tipo de anticuerpos (autoanticuerpos) que empeoran la infección, pues bloquean interferones como el IFN-ω y los IFN-α, que se relacionan con una peor respuesta inmunitaria innata, siendo esto un mal augurio pues desencadena un empeoramiento de la infección. En casos asintomáticos y personas sanas apenas se encontraron estos autoanticuerpos. En estos casos, el virus no es el responsable de la producción de estos anticuerpos que tienen un efecto negativo, sino que la producción de los mismos se debe a defectos genéticos congénitos del sistema inmune. Esto podría ser una de las causas de empeoramiento súbito en pacientes jóvenes sin patologías previas (ver estudio). También se comprobó que las personas de mayor edad tienen monocitos (glóbulos blancos) con menor capacidad de producir interferones (antivirales) que las personas más jóvenes, lo cuál también podría ser una de las claves que determine la evolución de la enfermedad junto con la carga viral.
Otro estudio llevado a cabo en Suecia encontró un hallazgo significativo, ya que se mostraron diferencias en las respuestas ofrecidas por las células NK (asesinas naturales) del sistema innato, cuya misión es localizar células infectadas y destruirlas. Estas células se activan fuertemente en las fases iniciales de la infección, pero se vio que actuaban de manera distinta en pacientes que cursaron la enfermedad de manera moderada y en pacientes con una clínica más severa. En los pacientes más graves, las células NK mostraron una mayor capacidad para eliminar células infectadas (ver artículo).
También llama la atención el hallazgo de un estudio, en pacientes mayores de 60 años, de que las mujeres presentan una respuesta inmunológica en general más robusta que los hombres; las mujeres crearon una respuesta con linfocitos T más potente y mantenida con la edad, mientras que en los hombres esa respuesta era más débil y disminuía a mayor edad. (ver estudio).
Hay científicos que indican que mientras que el virus de la gripe es devastador para las células humanas, puesto que en laboratorio puede acabar con ellas en menos de un día, el SARS-CoV-2 no lo es tanto, ya que muchas células infectadas en el laboratorio sobrevivían en el tiempo. Por tanto, el virus podría no ser tan agresivo como otros, pero sin embargo, se sospecha que jugaría un papel principal en el desenlace de la enfermedad el sistema inmunitario de cada persona, pues hay casos en los que se inicia un ataque desmesurado a través de la tormenta de citoquinas (ver noticia).





 Factores de riesgo
Factores de riesgo Técnicas de detección
Técnicas de detección Tratamientos
Tratamientos Vacunas
Vacunas Carga viral
Carga viral Mutaciones
Mutaciones Letalidad y mortalidad
Letalidad y mortalidad Prevención: mascarillas
Prevención: mascarillas Prevención: Ventilación y filtración (HEPA)
Prevención: Ventilación y filtración (HEPA) Otras medidas de prevención
Otras medidas de prevención Impacto de la pandemia
Impacto de la pandemia Fin de la pandemia
Fin de la pandemia Prevención en centros educativos
Prevención en centros educativos Enlaces de interés
Enlaces de interés





